NK细胞与肿瘤
NK 细胞在 20 世纪 70 年代首次被确认为一种独特的淋巴亚型细胞,能够在没有预先致敏或检测特定肿瘤抗原的情况下识别并快速杀死异常细胞,从而能够起到抗肿瘤作用。目前,基于自然杀伤(NK)细胞的免疫疗法已成为癌症免疫疗法中一个有前途的前沿科学研究课题。
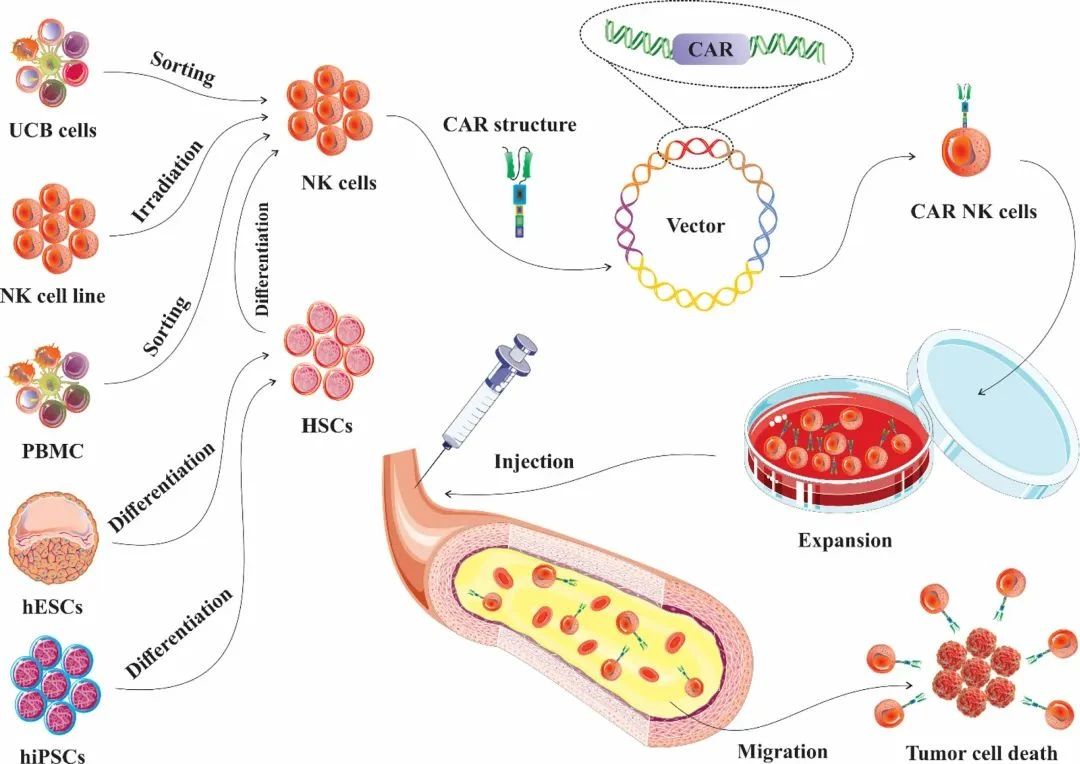
NK/CAR-NK 细胞的来源和生成过程
1. 通过NK膜表面的 Fc 受体CD16 在NK 细胞杀伤肿瘤细胞中起到重要作用,NK 细胞通过膜受体CD16 或通过FASL 和TRAIL 介导的凋亡途径引发 ADCC;
2. 诱导NK细胞向一种或多种TAAs 的BiKE 和TRiKEs 是治疗实体瘤的可行策略;
3. CARs将NK细胞重新定向到具有特异性抗原的肿瘤细胞上,能够精准清除肿瘤细胞。
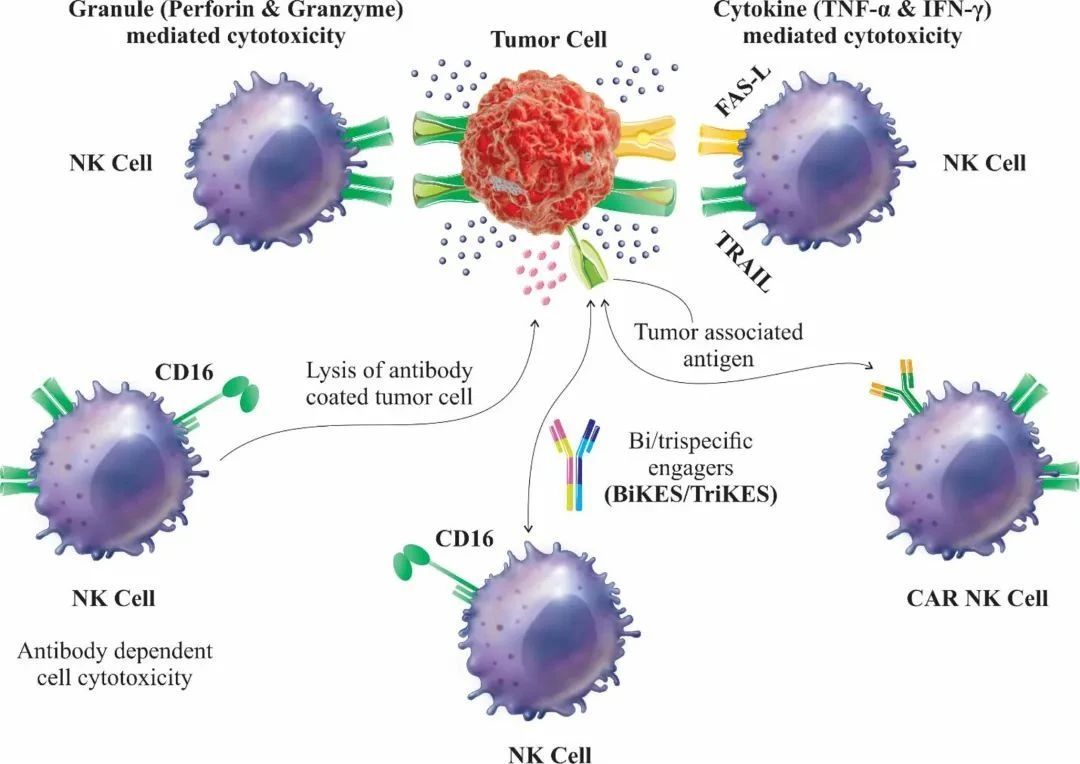
NK 细胞对肿瘤的细胞毒性机制
外周血来源NK细胞-80°C短期冻存
12周内NK细胞活性无明显变化
研究人员采集和分离健康人外周血单个核细胞,在体外培养扩增细胞,扩增12天后将部分NK细胞于-80C冻存1/4/12/24周。
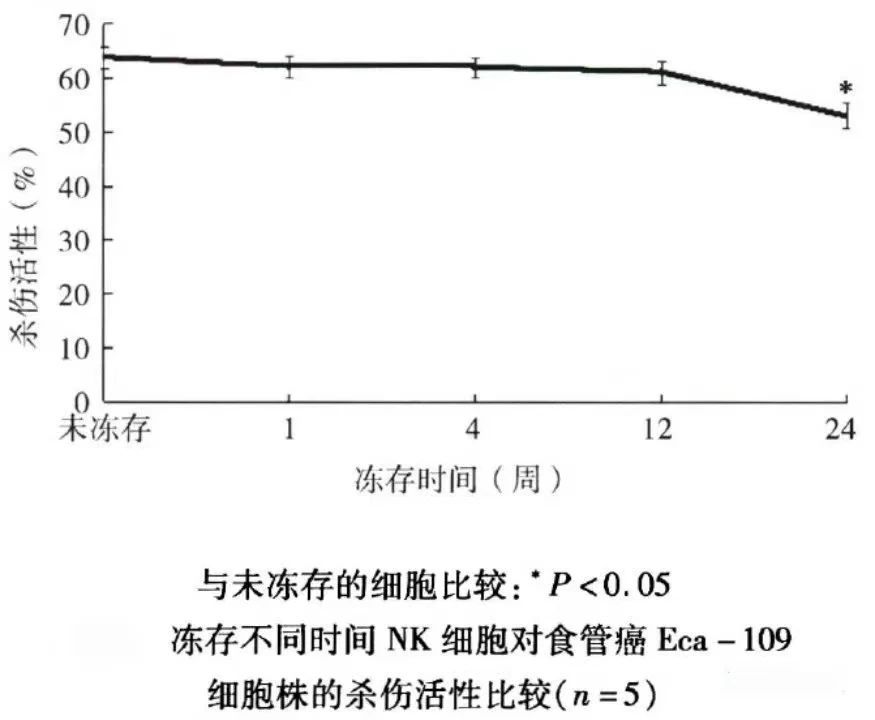
通过流式细胞仪分析冻存不同时间的NK细胞的表型、凋亡百分率、颗粒酶B、穿孔素及CD107a表达。如下图所示,-80°C冻存24周的NK细胞与未冻存的NK细胞的表型、活性、颗粒酶B、穿孔素及CDl07a表达相比,差异有统计学意义(P<0.05)。而-80°C冻存12周内的NK细胞与未冻存的NK细胞各组相比,差异无统计学意义(P>0.05)。
研究表明,-80°C冻存12周以内的NK细胞与未冻存的NK细胞比较,在表型和凋亡百分率方面均无明显变化,且细胞功能及杀伤活性也无明显改变,而肿瘤患者化疗的一个疗程大约为4周,因此-80°C冻存细胞可以满足大多数患者的需要。
脐带血来源的NK细胞冷冻10年
扩增能力和效应功能没有影响
脐带血(CB)是治疗性抗肿瘤效应NK细胞体外扩增的一个重要来源,从脐带血可以获得大量淋巴细胞效应细胞,这扩大了其临床潜力,甚至在治疗血液病方面超过了造血干细胞(HSC)移植。
比如,治疗性的离体扩增NK细胞可用于过继性细胞免疫疗法,可在临床上应用于治疗血液系统和实体恶性肿瘤。
全球范围内储存了超过600,000单位的脐带血,验证这种冷冻来源NK细胞的治疗能力非常重要。尽管已有研究证明了在造血干细胞移植中使用长期冷冻保存脐带血的临床功效,但对其用于效应免疫细胞离体扩增的效果却知之甚少。
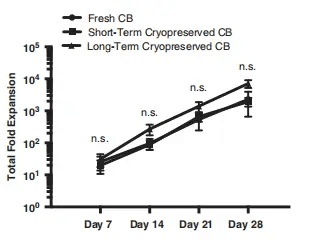
来自新鲜、短期冷冻保存或长期冷冻保存脐带血的CB-NK细胞具有类似的、稳健的对数规模扩增
研究人员从脐带血中分离并体外扩增了大量激活的NK细胞,根据冻存时间长短,将脐带血分为三个组别:长期组 (深低温冻存1-10年)、短期组(深低温冻存小于1年)、未冻存组(未经冻存的脐带血),然后对这些NK细胞杀伤乳腺癌细胞的作用进行了观察其扩增潜力和抗肿瘤效应功能。
研究发现,培养28天后,未冻存组、短期组、长期组的脐带血来源NK细胞都产生了类似的、稳定的指数级别扩增量,没有显著差异。同时离体扩增的脐带血来源NK细胞具有增加的激活标志物的表面表达,并通过产生稳定水平的促炎细胞因子,干扰素v和肿瘤坏死因子-a显示出有效的抗肿瘤功能。
文中所述这两种不同来源的NK细胞相比,脐带血来源的NK细胞收集和冷冻保存更加便捷,且长期冷冻保存对脐带血NK细胞的扩增潜能和抗肿瘤活性均没有影响。外周血NK细胞(不是PBMC)在短期(12周内)冻存是没有影响的,但再延长冻存期的话可能会显示一定的局限性。

