
2026年1月22日,斯坦福大学Michael T. Longaker团队在Cell 在线发表题为“Fibroblasts of disparate developmental origins harbor anatomically variant scarring potential”的研究论文。

科学家们通过精密的小鼠实验发现:面部伤口愈合后疤痕显著轻于头皮、腹部和背部等部位。这一现象背后的核心秘密,竟隐藏在皮肤中看似普通的“工人细胞”——成纤维细胞的发育起源中。
研究过程
该研究人员通过使用小鼠伤口模型,观察到面部伤口的疤痕形成比头皮、腹侧和背侧伤口要少。单细胞 RNA 测序显示,与来自其他部位的纤维细胞相比,神经嵴衍生的面部纤维细胞中 Robo2 和下游的 Eid1 的表达增加。
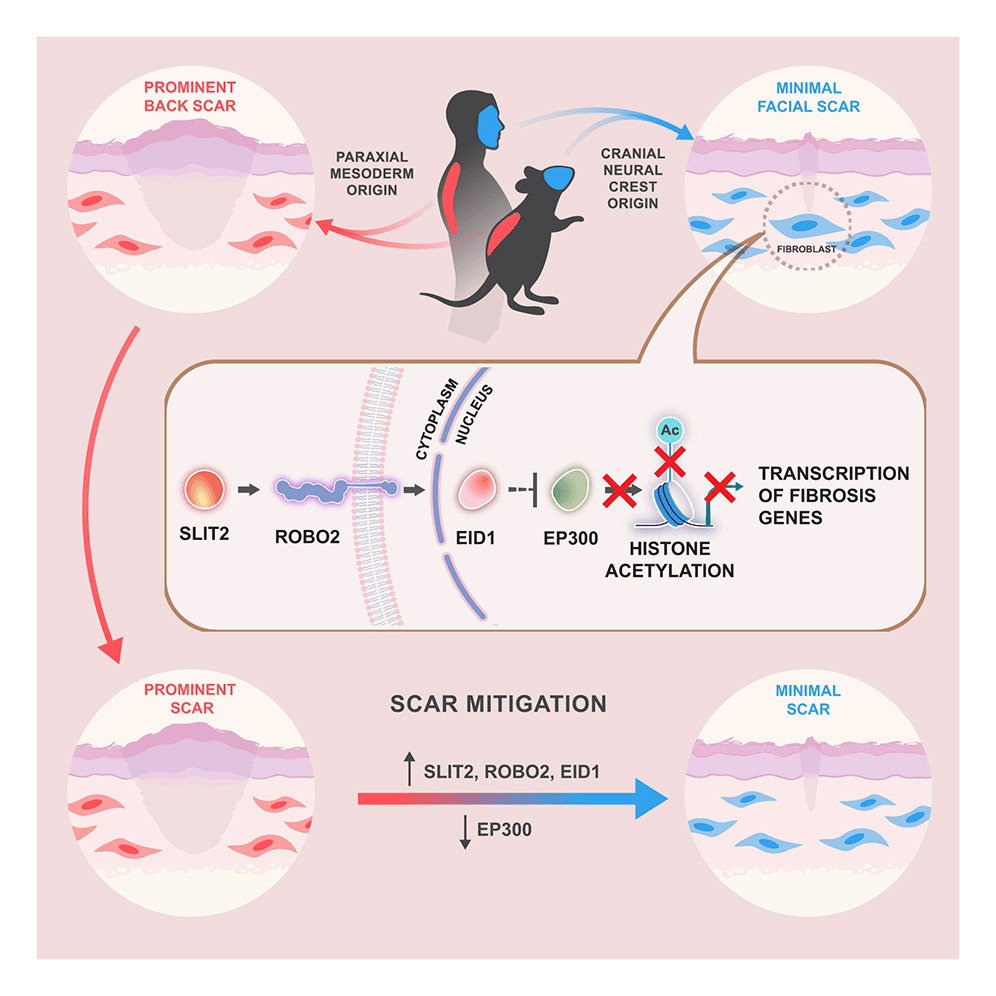
在纤维细胞移植实验中,Robo2 和 Eid1 促进了面部纤维细胞降低的疤痕形成潜力。这是通过抑制 EP300 组蛋白乙酰转移酶来维持的,从而导致更沉默的转录组染色质景观。模拟 EID1 的活性,对背侧伤口中的小分子和转基因 EP300 抑制物促进了具有面部样特征的愈合,同时减少了疤痕形成。这些数据突显了 ROBO2-EID1-EP300 信号通路在面部伤口愈合过程中的重要性,并展示了能够调控成纤维细胞的胚胎决定型促纤维化潜能,从而最大程度减少疤痕形成的能力。
证据表明,成纤维细胞的异质性可能意味着存在导致不同疤痕形成的内在纤维细胞特性。来自不同人体部位的成纤维细胞具有独特的位置特性,这些特性是由不同的基因表达程序所决定的,其中包括对胚胎发育中轴形态形成至关重要的 HOX 基因。此外,皮肤成纤维细胞的胚胎起源取决于其所在的位置:面部、头皮、腹侧和背侧的成纤维细胞主要来自颅神经嵴、头段中胚层、侧板中胚层和脊索中胚层。这些成纤维细胞的起源反过来可能会影响其在出生后的纤维化行为。
该研究提供了相关证据,表明面部成纤维细胞具有较低的纤维化潜能,这与其神经嵴起源有关。该研究发现,与来自其他解剖部位的成纤维细胞相比,面部成纤维细胞会上调 SLIT2-OBO2信号通路,该通路在神经嵴细胞生物学中起着重要作用,从而促进伤口愈合并减少纤维化。SLIT2-ROBO2 通过 EID1 介导的抑制 EP300 来维持染色体处于更转录沉默的状态。在成纤维细胞中对 SLIT2 - ROBO2 - EID1 轴进行基因和小分子操作,使得背侧伤口(DWs)能够像面部伤口(FWs)一样愈合,且疤痕减少,这表明有能力利用成年成纤维细胞的固有可塑性来开发抗纤维化疗法。
疤痕轻重与成纤维细胞的“出生地”直接相关
胚胎发育溯源:
面部皮肤(尤其是口鼻区域)的成纤维细胞主要来源于胚胎期的颅神经嵴。
而头皮、腹部、背部的成纤维细胞则主要来源于中胚层。
功能差异显著:
颅神经嵴来源的成纤维细胞:在伤口愈合过程中,展现出独特的“低瘢痕化”潜能。它们倾向于产生更纤细、排列更有序的胶原蛋白(I型和III型),更接近正常皮肤结构,同时能更有效地重塑细胞外基质
中胚层来源的成纤维细胞:则更容易驱动过度纤维化。它们产生的胶原蛋白更粗壮、排列更紊乱(形成典型的疤痕组织束),且细胞外基质重塑能力较差,导致增生性疤痕或瘢痕疙瘩风险更高。
纤维化是全球范围内导致疾病发生和死亡的主要原因,在美国,其导致的死亡人数占比高达 45%。在皮肤上,纤维化会导致严重的心理和社会压力以及功能障碍。尽管纤维化现象普遍存在且导致了大量疾病,但目前的临床治疗方法都无法完全预防或逆转这一纤维化过程。
神经嵴由一种多能干细胞样群体组成,它构成了颅面部骨骼和结缔组织。神经嵴细胞及其衍生物都具有显著的可塑性。
成纤维细胞治疗疤痕的核心机制:从"失控"到"调控"
成纤维细胞治疗疤痕的核心,在于通过各种手段对异常的成纤维细胞进行调控,使其恢复正常的功能状态,或者利用具有特定功能的成纤维细胞来修复受损组织,实现疤痕的淡化甚至消除。
01抑制成纤维细胞过度增殖与胶原合成
1:糖皮质激素干预:疤痕封闭针是临床常用的治疗手段,其核心成分糖皮质激素(如曲安奈德)能够直接作用于成纤维细胞,抑制其增殖活性,减少胶原蛋白的合成。同时,糖皮质激素还能上调基质金属蛋白酶(MMPs)的活性,促进过量胶原的降解,使疤痕组织逐渐变软、变平。此外,它还可以抑制局部炎症反应,减少炎症因子对成纤维细胞的刺激,从而打破疤痕增生的恶性循环。
2:压力治疗的生物力学调控:压力治疗作为预防和治疗增生性疤痕的基石性方法,其作用机制也与成纤维细胞密切相关。持续、均匀的压力能够机械性抑制成纤维细胞的增殖,减少胶原的合成。同时,压力可以引导新合成的胶原纤维沿压力方向重新排列,从杂乱的结节状转变为接近正常皮肤的平行束状,改善疤痕的质地和外观。此外,压力还能压迫微血管,减少疤痕的血液灌注,降低局部组织的氧分压,相对缺氧的环境也能抑制成纤维细胞的过度功能。
02促进成纤维细胞的正常分化与组织再生
1:面部成纤维细胞的再生特性启示:斯坦福大学Michael T. Longaker团队的研究发现,面部伤口愈合后疤痕较少,与面部成纤维细胞的独特特性密切相关。面部成纤维细胞源自神经嵴细胞,高表达ROBO2蛋白及其下游因子EID1,这一信号通路能够抑制EP300蛋白质的功能,使DNA保持相对"沉默"和紧密的状态,从而抑制促纤维化基因的表达,让面部细胞倾向于再生修复而非疤痕修复。这一发现为疤痕治疗提供了新的思路,即通过调控成纤维细胞的基因表达,使其模拟面部成纤维细胞的再生模式,实现无疤痕愈合。
2:自体成纤维细胞移植技术:成纤维细胞技术是一种新兴的疤痕治疗方法,其原理是利用皮肤成纤维前体细胞制备自体成纤维细胞,然后将其移植到疤痕组织处。这些移植的成纤维细胞能够持续产生胶原蛋白,补充真皮层的厚度,恢复皮肤的弹性和光泽,从而抚平皱纹和凹陷性疤痕。与传统治疗方法相比,自体成纤维细胞移植具有生物相容性好、无免疫排斥反应等优点,能够从根本上改善疤痕组织的结构和功能。
03调控成纤维细胞相关信号通路
1:ROBO2-EID1-EP300信号通路:如前文所述,ROBO2-EID1-EP300信号通路在面部无疤痕愈合中发挥着关键作用。通过激活这一信号通路,可以抑制成纤维细胞的纤维化倾向,促进其向再生方向分化。研究人员已经尝试使用针对EP300的小分子抑制剂,在小鼠背部伤口上模拟出面部细胞的愈合模式,显著减少了疤痕的形成。这为临床治疗疤痕提供了新的药物靶点,有望开发出更加有效的抗疤痕药物。
2:Engrailed-1(En1)信号通路:斯坦福大学的另一项研究发现,防止成纤维细胞中的En1激活,可以实现伤口的再生而不留下疤痕^。在疤痕形成过程中,皮下筋膜中的En1阳性成纤维细胞会移动到受损处,促进疤痕组织的形成。而通过阻断机械转导信号传导,如使用Yes相关蛋白(YAP)的抑制剂或成纤维细胞特异性转基因YAP基因敲除,可以阻止En1激活,促进En1阴性成纤维细胞介导的伤口再生,恢复皮肤的正常结构和功能。
Longaker团队的研究如同一把钥匙,打开了理解皮肤“地域性”愈合差异的大门。它揭示了成纤维细胞并非千篇一律的“修补工”,它们的“出身”深刻烙印在功能上,决定了疤痕的轻重。这一发现不仅解答了基础生物学问题,更为攻克困扰医学界的疤痕难题——从烧伤、创伤到外科手术切口——提供了革命性的思路和充满希望的靶点。未来,我们或许能真正实现“无痕愈合”的梦想。
参考文献
1:cell-Fibroblasts of disparate developmental origins harbor anatomically variant scarring potential
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

