
圣路易斯华盛顿大学医学院的研究人员在2021年发表于《临床癌症研究》期刊的题为“Memory-like Differentiation Enhances NK Cell Responses to Melanoma”的研究中,探讨了记忆样分化如何增强自然杀伤细胞(NK细胞)对黑色素瘤的反应。该研究由Nancy D. Ma等人完成,重点在于开发针对晚期黑色素瘤的新型免疫疗法。

将对照和ML NK细胞过继转移到NSG小鼠体内NOD-scid IL2Rγnull(NSG)小鼠(6-10周龄;Jackson Laboratories)在第0天用250 cGy照射并注射1×105 DM6-RhoC-Luc(腹膜内)。在第1天,将如图3A所示产生的500万个对照或预激活的NK细胞腹膜内注射到荷瘤小鼠体内。在腹腔注射NK细胞之前,通过生物发光成像(BLI)确认小鼠是否存在肿瘤,并在实验期间每周成像一次。每隔一天腹腔注射rhIL2(50000IU)以支持转移的细胞。
表明未成熟的CD56brightCD16-NK细胞是晚期黑色素瘤淋巴结中的主要群体。因此,NK细胞渗透到晚期黑色素瘤环境中,并表现出降低的细胞毒性潜力,GzmB和穿孔素的表达降低,这一缺陷可以通过过继性NK细胞疗法来解决。
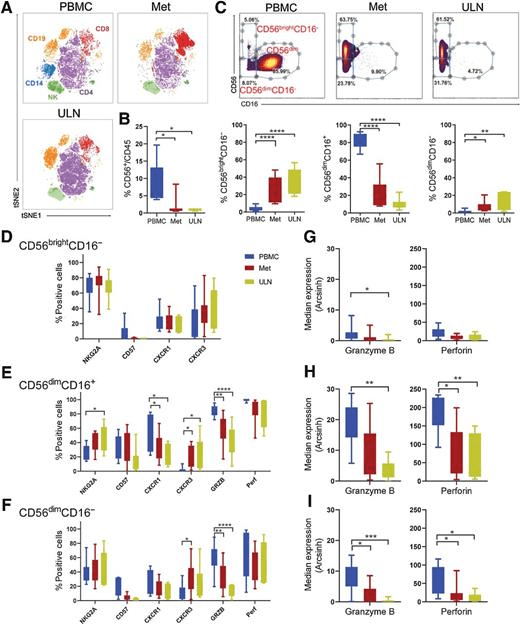
浸润转移性黑色素瘤的NK细胞大多是未成熟的CD56bright和不太常见的成熟CD56dim NK细胞,它们表现出减少的细胞毒性分子。A,viSNE图的代表性示例,显示了晚期黑色素瘤患者PBMC、转移性(Met)和ULN中主要免疫亚群的分布。B,CD45+细胞内NK细胞(CD56+CD3-)的百分比。C,根据CD56和CD16的表达确定了三种NK细胞亚群:CD56bright、CD56dimCD16+和CD56dimCD 16-,并显示了它们在总NK细胞中的频率。D,使用质量细胞术分析NK细胞相关标志物的表达(见补充表S2)。D-F、成熟标志物(NKG2A、CD57)、趋化因子受体(CXCR1、CXCR3)和CD56bright、CD56dimCD16+和CD56dimCD 16-中的功能相关分子(GRZB、Perf)通过质量细胞术进行评估。
研究对11名晚期黑色素瘤患者和15名HD患者的血液NK细胞进行了比较表型分析,以确定晚期黑色素癌患者的NK细胞多维表型。晚期黑色素瘤和HD之间的总NK细胞频率没有差异。然而,在黑色素瘤患者中,CD56dimCD16−减少,CD56dim CD16+NK细胞频率增加(补充图S3A和S3B)。数据表明晚期黑色素瘤患者的血液NK细胞具有降低的激活受体表达和细胞毒性潜力。这种功能改变在晚期黑色素瘤中更为明显——驻留的NK细胞表明,有效的自体反应需要增强NK细胞抗黑色素瘤活性的方法。
来自同一HD的ML NK细胞在用DM6和M14黑色素瘤细胞重新刺激后,IFNγ、TNF和CD107a的表达显著增加(图2B-E)。当使用纯化的NK细胞代替PBMC时,ML NK细胞的卓越细胞因子反应和脱颗粒也很显著(补充图S4A-S4C)。与脱颗粒增加一致,HD的ML NK细胞也表现出显著增加和持续的细胞毒性,从而即使在低E:T比值下也能消除黑色素瘤靶细胞(图2E和F)。这些结果支持ML NK细胞在体外控制黑色素瘤靶点的能力显著增强。
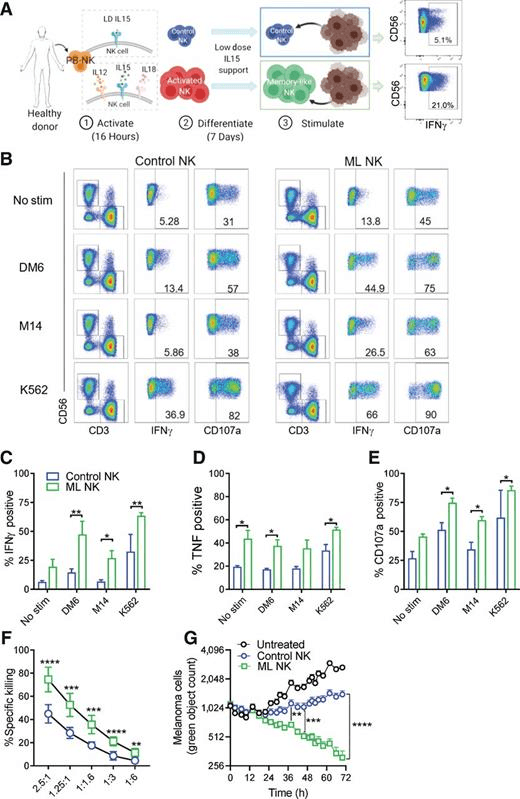
在标准的4小时51Cr释放试验(F)和72小时Incucyte试验(G)中,ML NK细胞对DM6的杀伤能力优于对照NK细胞
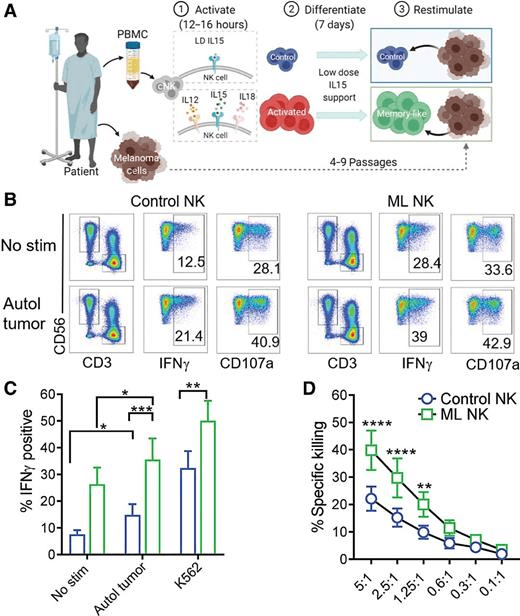
如图3A所示,对晚期黑色素瘤患者(n=7;补充表S1)的PBMC进行刺激,使其NK细胞分化为ML NK细胞(图3A)。转移性病变产生的自体原发性黑色素瘤细胞被用作功能检测的靶标。对于所有患者,S100、MelaA和SOX10的IHC染色证实这些细胞系是转移性黑色素瘤(补充图S5)。当用自体黑色素瘤靶点重新刺激时,ML NK细胞与对照NK细胞相比,IFNγ的产生显著增加(图3B和C)。与HD的ML NK细胞相比(图2),晚期黑色素瘤患者的自体ML NK细胞也表现出基线IFNγ产量的增加。与对照NK细胞相比,晚期黑色素瘤患者的ML NK细胞对自体黑色素瘤细胞的特异性杀伤也显著增加,即使在低E:T比值下也是如此(图3D)。
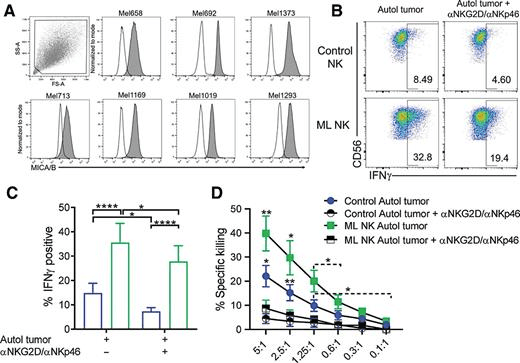
晚期黑色素瘤患者的ML NK细胞对晚期黑色素癌靶点的增强反应依赖于NKG2D和NKp46。用DM6刺激HD纯化的NK细胞后,发现细胞因子反应、脱颗粒和杀伤也出现了类似的减少,这表明对NK细胞有特异性作用(补充图S6F-S6I)。重要的是,同时阻断NKG2D和NKp46而不是单一阻断显著影响了NK细胞功能的降低(补充图S6J和S6K)。这些结果共同证明了NKG2D和NKp46在增强ML NK细胞对自体黑色素瘤靶点的反应中的关键作用。
使用免疫缺陷NSG小鼠的人异种移植物模型评估人ML NK细胞在体内控制黑色素瘤靶点的能力。NSG小鼠注射1×105 DM6-RhoC-Luc细胞(腹膜内),1天后小鼠单次注射5×106对照NK细胞或ML NK细胞(腹膜外)。由于NSG小鼠缺乏支持NK细胞存活和扩增所需的稳态IL2/15R配体,因此每隔一天(腹膜内)注射IL2(50000IU/小鼠)以支持转移的人NK细胞,并每周通过BLI监测黑色素瘤负荷(图5A)。与未治疗的小鼠相比,接受对照NK细胞的小鼠能够显著控制黑色素瘤肿瘤负荷,尽管肿瘤会随着时间的推移而发展。相比之下,用单剂量ML NK细胞(来自同一供体)过继转移的小鼠在体内控制黑色素瘤细胞的能力明显优越,在实验期间肿瘤负荷得到控制(图5B和C)
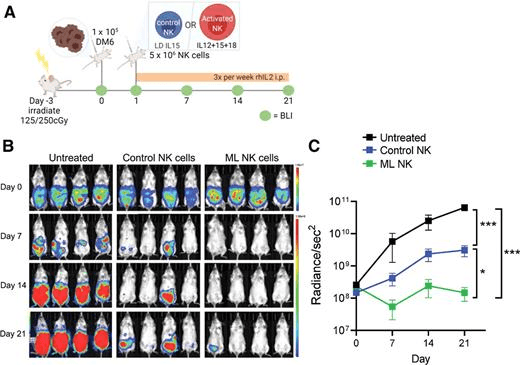
证明了IL12、IL15和IL18受体诱导的HD和晚期黑色素瘤患者的ML NK细胞具有更强的攻击黑色素瘤靶点的能力。患者血液NK细胞的ML分化导致产生IFNγ和杀死自体黑色素瘤靶点的能力增强。
因此,来自功能失调的晚期黑色素瘤或HD患者的NK细胞的ML分化代表了增强NK细胞抗黑色素瘤攻击的新方法,并值得作为细胞疗法进行进一步研究。
针对PD-1和CTLA-4的免疫检查点阻断(ICB)疗法作为单一或联合疗法,已经彻底改变了包括黑色素瘤在内的多种癌症类型患者的治疗。阻断这些抑制性受体可增强T细胞介导的抗肿瘤免疫反应,从而改善晚期黑色素瘤患者的临床反应和生存率。然而,尽管取得了成功,但免疫和药物相关的不良反应很常见,影响了50%以上接受联合治疗的患者。此外,超过50%的患者从未有过反应,大约50%的最初有反应的患者会产生耐药性,最终发展为进行性疾病。此外,对于BRAF突变型黑色素瘤患者,仅靶向治疗就能提高生存率;然而,这并不能治愈。肿瘤的内在和外在机制与ICB的耐药性有关,包括肿瘤细胞下调MHC-I抗原呈递途径以逃避细胞毒性T细胞抗原特异性免疫反应。NK细胞已成为治疗癌症患者的一种有前景的疗法,因为它们是安全的,并发挥强大的抗肿瘤反应。
总之,ML NK细胞在临床前实验中表现出增强的体内和体外控制黑色素瘤靶点的能力。重要的是,证明了ML分化程序可以挽救晚期黑色素瘤患者中功能失调的NK细胞,并且患者来源的ML NK细胞可以有效地控制自体肿瘤。
什么是黑色素瘤
黑色素瘤是一种侵袭性癌症,由于该疾病的侵袭性变体具有高复发风险和快速进展过程,因此仍然是一个临床挑战。靶向和免疫治疗方法彻底改变了晚期黑色素瘤的治疗。特别是,针对CTLA-4和PD-1的免疫检查点阻断抗体的引入显著提高了晚期或转移性黑色素瘤患者的生存率。然而,尽管取得了这些进展,但仍有50%以上的患者对检查点阻断无效。此外,在最初对检查点阻断有反应的患者中,约有50%复发,这突显了探索替代免疫疗法的必要性。
NK细胞免疫系统的“第一道防线”
NK细胞是先天性免疫的核心成员,通过识别激活性与抑制性受体的平衡决定是否杀伤异常细胞。其优势在于无需抗原预致敏,可快速响应肿瘤细胞。然而,在黑色素瘤微环境中,NK细胞常因活化受体表达降低和细胞毒性减弱而功能耗竭。
记忆样分化的革命性发现
Ma团队通过质谱技术发现,晚期黑色素瘤患者的NK细胞中,颗粒酶B(GzmB)等关键效应分子表达显著下降,导致其无法有效杀伤癌细胞。研究创新性地提出:
细胞因子诱导记忆化:用IL-12、IL-15和IL-18短暂激活NK细胞,可促使其分化为记忆样(ML)NK细胞,这种细胞在再次接触相同抗原时,能产生更强烈的细胞毒性和干扰素γ(IFN-γ)分泌。
功能增强机制:记忆样NK细胞通过表观遗传重编程,获得类似适应性免疫的“记忆”特性,对黑色素瘤细胞的杀伤效率显著提升。
细胞攻瘤的“智能导航”系统
研究发现,ML NK通过双重机制精准锁定黑色素瘤:
01 靶向识别
高表达NKG2D受体,特异性结合肿瘤细胞应激分子MICA/B
02穿透屏障
分泌基质金属蛋白酶(MMP),瓦解肿瘤纤维化屏障
动物实验显示:接受ML NK治疗的小鼠肿瘤负荷下降92%,肺转移灶减少87%
通过细胞因子诱导分化(IL-12/15/18),普通NK细胞可转化为具有“免疫记忆”特性的记忆样NK细胞(ML NK)。这种改造赋予细胞
三大核心优势:
1. 长效持久性:体内存活时间延长3倍以上
2. 超强增殖力:扩增能力提升5-8倍
3. 精准杀伤力:黑色素瘤清除率提升76%
结 语
尽管该研究仍处于临床前阶段,但记忆样NK细胞疗法已展现出成为“通用型”免疫疗法的前景。其无需基因改造的特性,可大幅降低生产成本,为全球患者带来可及性更高的治疗选择。随着临床试验的推进,这一技术有望重新定义晚期黑色素瘤的治疗格局。
参考文献
1:Memory-like Differentiation Enhances NK Cell Responses to Melanoma
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

