
在快节奏的现代生活里,“不吃早餐”似乎成了不少人的常态。有人为了多睡几分钟,有人觉得能节省时间,还有人想借此控制体重。
来自浙江大学医学院王迪课题组、浙江大学爱丁堡大学联合学院研究员刘琬璐课题组等的研究人员,在顶刊Cell发表了一篇题为“A two-front nutrient supply environment fuels small intestinal physiology through differential regulation of nutrient absorption and host defense”的研究论文,绘制了小肠双向营养供给环境的全面、高分辨率图谱,可视化了营养吸收的时空动力学和细胞类型趋向性等核心特征,并发现“不吃早餐”的生活方式,会导致小肠细胞脂质过度吸收,从而增加代谢疾病的风险。

要理解不吃早餐的危害,首先得认识小肠这个人体营养吸收的核心器官。小肠不仅是消化食物、吸收营养的主要场所,还承担着激素分泌、免疫防御等重要功能。更神奇的是,它拥有独特的双向营养供给机制——一方面从肠腔内侧吸收食物中的营养,另一方面通过浆膜侧的血管获取来自其他器官的循环代谢物。这两种营养供给路径相互配合,共同维持着小肠的正常生理功能和人体的代谢稳态。
实验过程
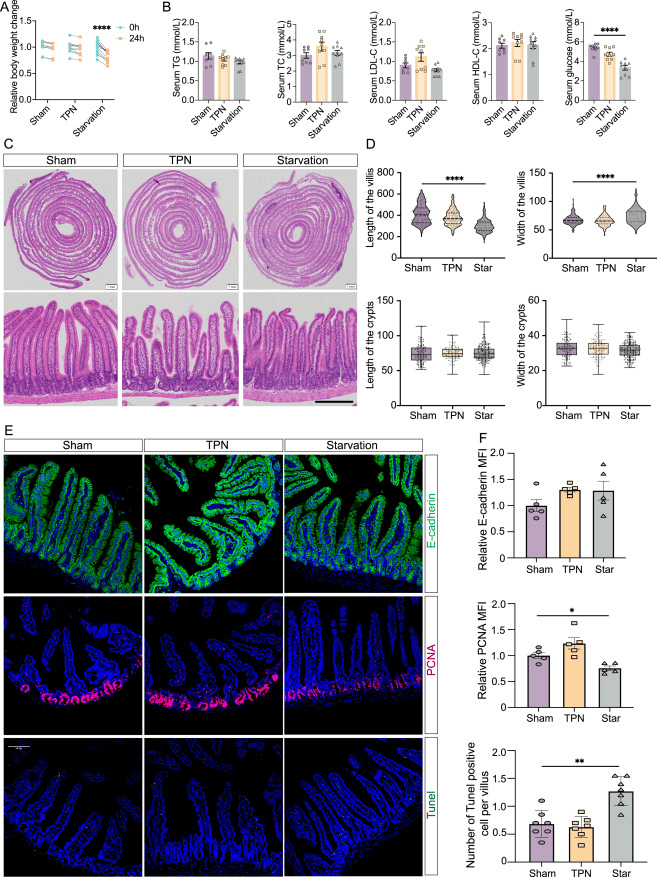
为了全面研究小肠双向营养供给的奥秘,研究团队设计了三种小鼠喂养模型,其中小肠由不同供应来源的营养物质提供能量(图1A,左)。在24小时的适应期内,所有小鼠都随意喂食正常食物(NC)和连续尾静脉输注4.8 mL/天的生理盐水。在空肠组织采集前的24小时内,假手术组的小鼠保持其原始喂养状态。作为一种绕过胃肠道并作为唯一外部营养来源的喂养方法,全胃肠外营养(TPN)组的小鼠被剥夺了食物,但接受了尾静脉输注的TPN,每天提供约5.8千卡和30毫克氮,以满足随意喂养的小鼠的需求。14在饥饿组,小鼠被剥夺食物,并继续尾静脉输入生理盐水。24小时后,TPN组的体重(图S1A)、指示全身代谢的血清代谢物水平(图S1B)以及绒毛的解剖结构和细胞规律与假手术组相当(图S1C-S1F)。
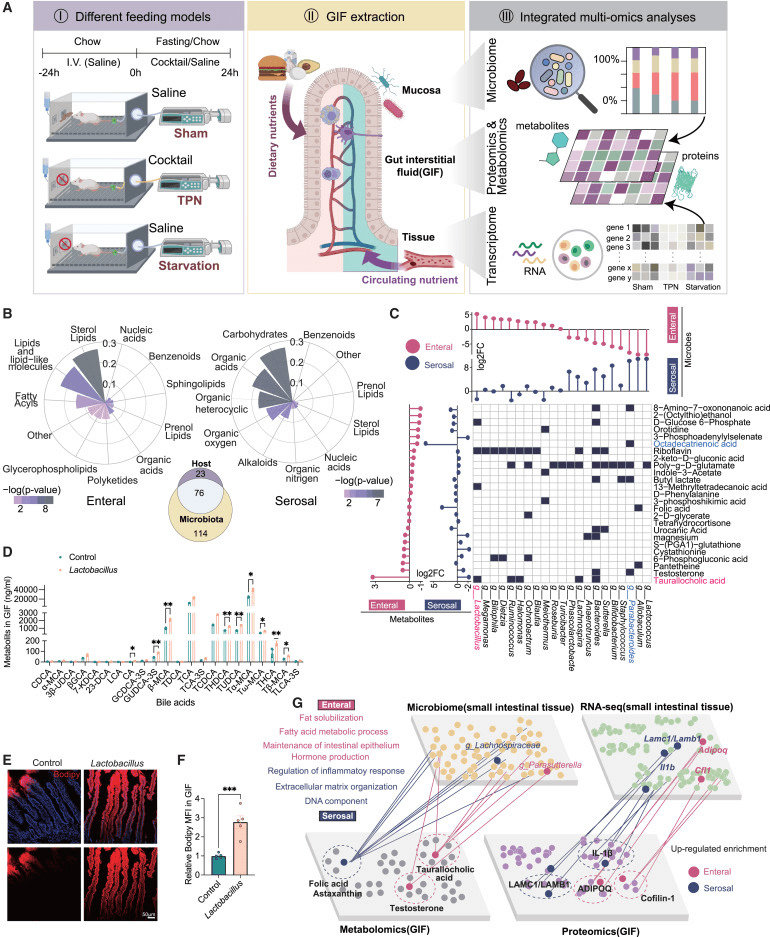
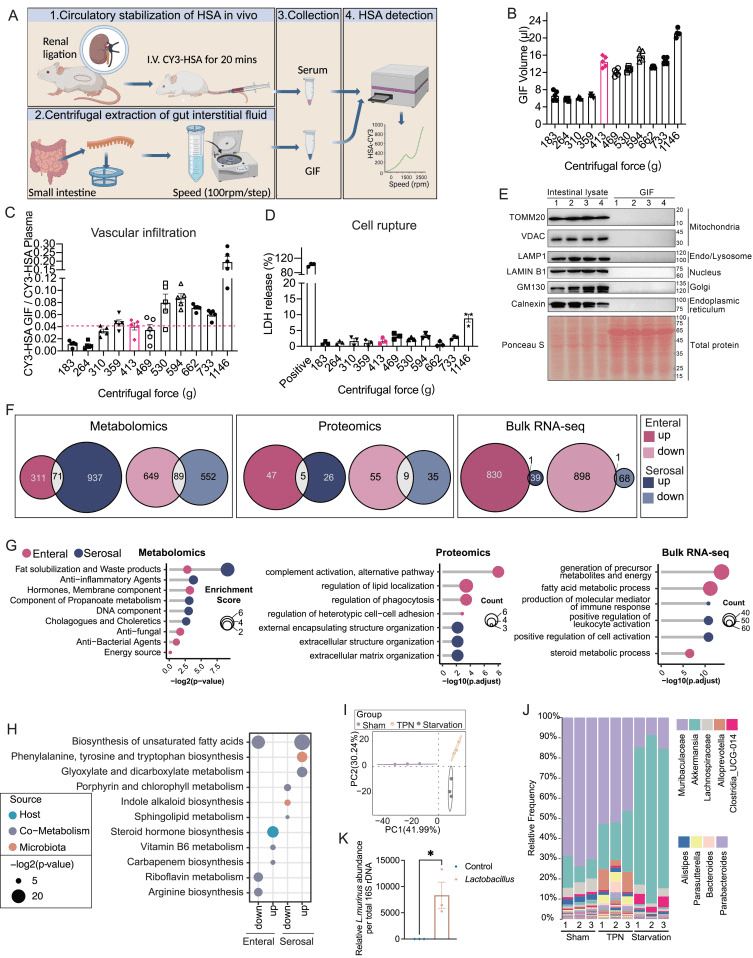
通过无偏代谢组学和定量蛋白质组学分析分析了GIF内容物的组成,并分别通过16S核糖体DNA测序(rDNA-seq)和体RNA测序(RNA-seq)对空肠组织的粘膜相关微生物组和肠道转录组进行了表征。然后应用深入的跨尺度生物信息学分析,将这些微生物和细胞信息与GIF代谢组学和蛋白质组学数据集整合在一起(图1A,右)。
对物种起源的分析表明,这些GIF代谢物中有相当一部分是由微生物群产生的(图1B),这表明微生物群衍生的代谢物对小肠的细胞外空间环境做出了重大贡献。代谢富集途径分析显示,浆膜侧上调的GIF代谢物优先富集在与合成代谢相关的途径中,如脂肪酸和氨基酸生物合成(图S2H)。相比之下,肠侧似乎更倾向于积累类固醇激素生物合成的代谢物(图S2H)。通过16S rRNA基因测序,然后基于加权UniFrac距离进行主成分分析(PCA),我们发现组间空肠微生物群含量发生了显著变化(图S2I和S2J)。
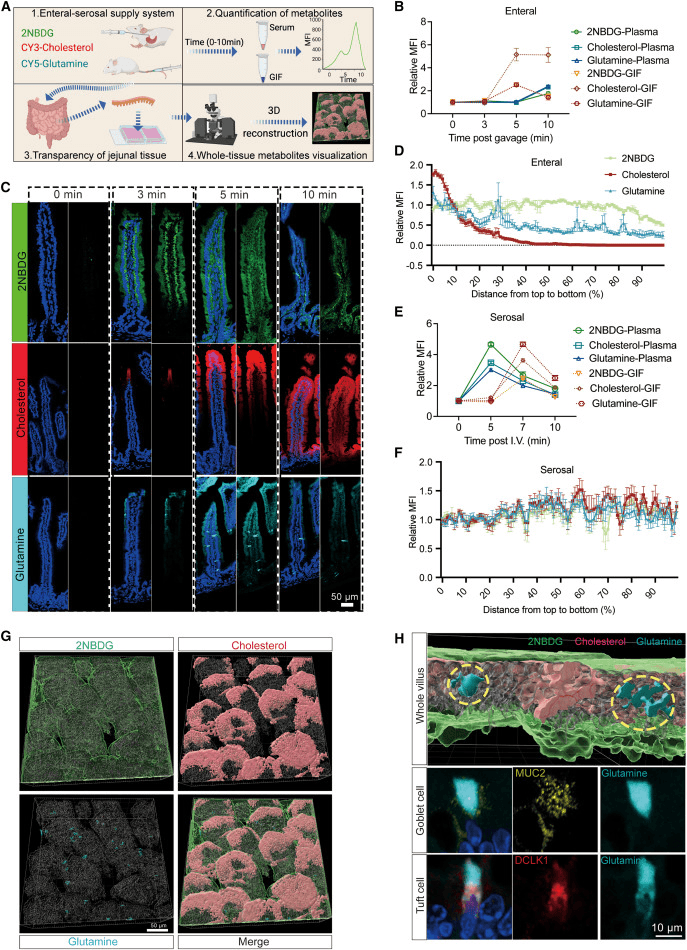
相比之下,浆膜侧似乎对肠道组织结构和细胞适应性的基本支持有更大的影响,如细胞外基质组织和DNA成分,以及免疫调节(图1G和S2G)。通过荧光显微镜观察了绒毛内荧光标记营养物的时空分布。在通过肠侧吸收葡萄糖的过程中,2-NBDG的荧光信号在灌胃后3分钟主要集中在上皮层,然后在5分钟扩散到固有层区域(图2C)。胆固醇和谷氨酰胺在绒毛中的吸收略晚于葡萄糖(图2C)。
营养素通过浆膜侧静脉注射到小肠中时,分别在注射后5分钟和7分钟在血清和GIF样本中检测到它们的显著荧光信号(图2E)。由于全身消耗,血清中的信号迅速下降,GIF样本中的信号在注射后10分钟也下降了(图2E),这意味着它们被小肠中的局部细胞吸收。与肠侧不同,浆膜侧对这些营养素的吸收模式相似,绒毛沿线没有明显的区域或细胞类型特异性(图2F和S3A)。
在假手术组中,杯状细胞与邻近的肠上皮细胞相比表现出更高的谷氨酰胺积累(图3B),而TPN组的这种积累显著减少,饥饿组的这种累积进一步减少(图3C)。在细胞内被吸收后,谷氨酰胺为碳和氮代谢途径提供燃料,包括三羧酸(TCA)循环、核苷酸合成和谷胱甘肽(GSH)合成。值得注意的是,与假手术组相比,TPN组杯状细胞中参与关键抗氧化剂GSH合成的一系列代谢物的水平同时降低,包括谷氨酸、还原型GSH和半胱氨酸甘氨酸(图S4A)。
为了探索肠内谷氨酰胺摄取在粘液产生中的作用,研究人员用无谷氨酰胺(Gln-)饮食喂养小鼠4周。用PAS/AB和Carnoy固定剂或抗Muc2抗体对粘蛋白进行染色时,NC组的小肠间充满了粘液,而Gln−组的这些信号大大减弱(图3D和3E)。使用组织透明技术和共聚焦3D成像,利用微球的聚集界面来描绘粘液层的表面。
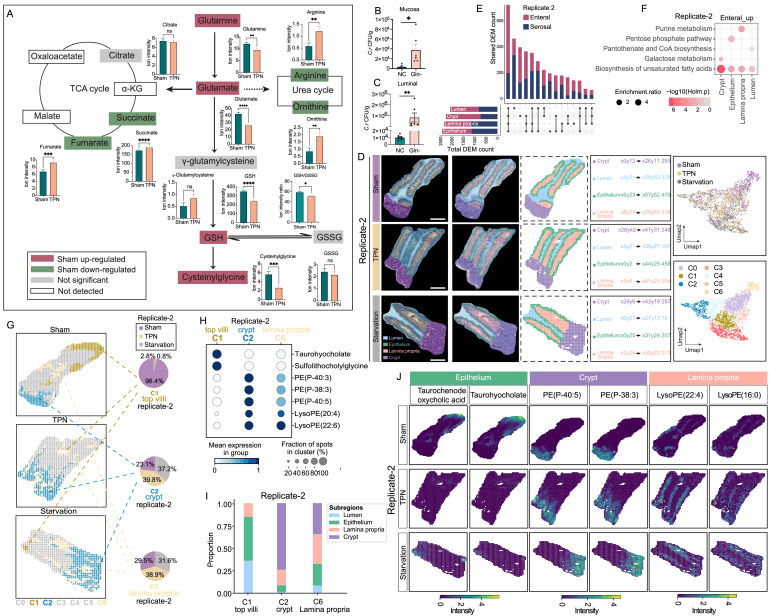
结果显示,NC组的微球被绒毛外的粘液层堵塞,而Gln-组的微球直接穿过绒毛间隙并与绒毛表面直接接触(图3F和3G)。小肠粘液层的松散性质为共生细菌的定植提供了有利的环境,同时防止上皮细胞直接被致病菌入侵。
研究人员观察到在Gln组中,一些细菌直接粘附在上皮表面,而没有被粘液层隔开(图3H)。当小鼠感染病原体C.rodentium(C.r)时,我们观察到在灌胃感染的第4天,Gln−组的肠道C.r负荷显著增加,尤其是小肠(图3K、3L、S4B和S4C)。这些发现共同强调了饮食中谷氨酰胺摄取在促进杯状细胞粘液产生中的关键作用。
基于H&E染色,研究人员将空肠组织分为四个不同的亚区:隐窝、固有层、上皮和管腔区域(图3M和S4D)。两个营养供应侧在所有次区域都产生了大量的差异富集代谢物(DEM)(图3N和S4E)。随后对上调的DEMs进行富集分析表明,与脂质代谢相关的途径在所有亚区都显著富集,以响应肠内营养(图3O和S4F)。
为了探索肠内谷氨酰胺摄取在粘液产生中的作用,我们用无谷氨酰胺(Gln-)饮食喂养小鼠4周。当用PAS/AB和Carnoy固定剂或抗Muc2抗体对粘蛋白进行染色时,NC组的小肠间充满了粘液,而Gln−组的这些信号大大减弱(图3D和3E)。
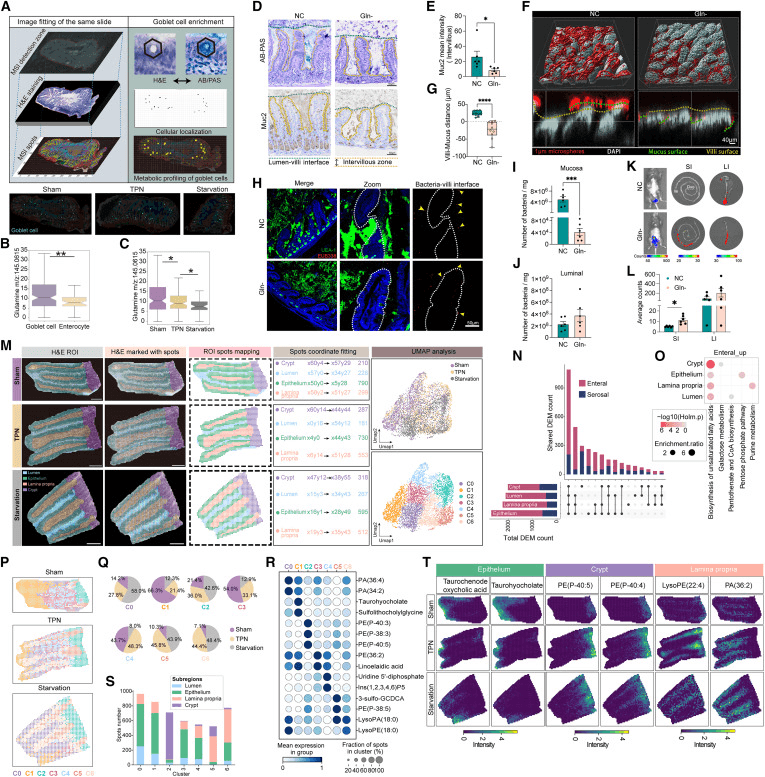
研究人员观察到在Gln组中,一些细菌直接粘附在上皮表面,而没有被粘液层隔开(图3H)。当小鼠感染病原体C.rodentium(C.r)时,观察到在灌胃感染的第4天,Gln−组的肠道C.r负荷显著增加,尤其是小肠(图3K、3L、S4B和S4C)。这些发现共同强调了饮食中谷氨酰胺摄取在促进杯状细胞粘液产生中的关键作用。
TPN对上皮更新的基本支持。为了验证这一点,使用了体内5-乙炔基-2'-脱氧尿苷(EdU)染色法,发现尽管与假手术组相比,TPN组绒毛区域的EdU+细胞较少,但与饥饿组相比,TPN组的EdU+细胞仍然明显更多(图S5B和S5C)。
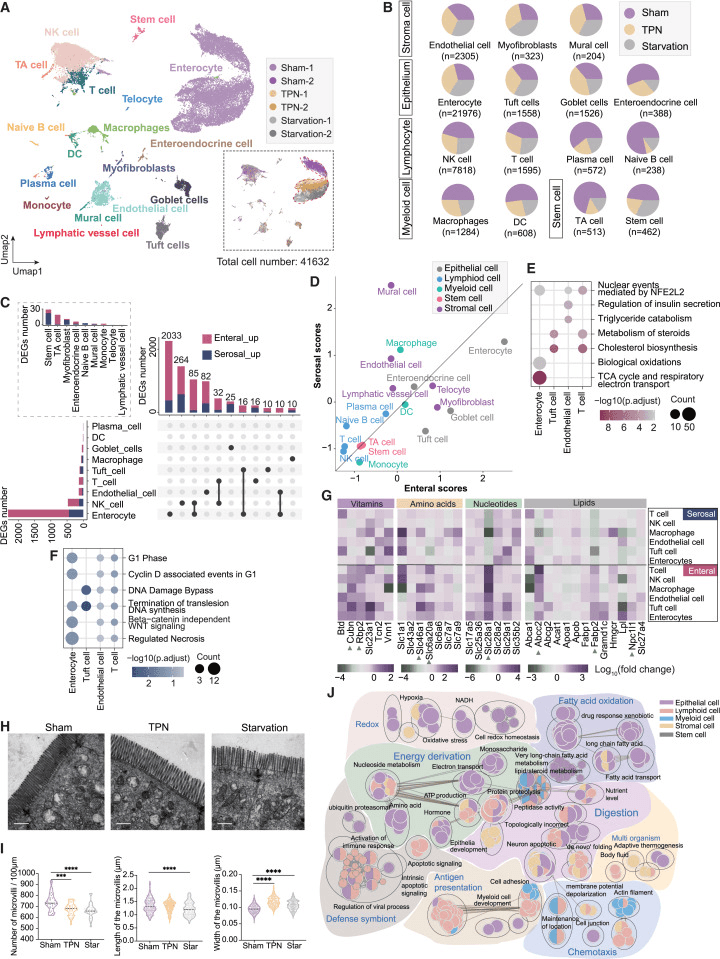
浆膜供应侧富集了相对较少的GO术语模块,这些模块主要代表上皮细胞的基本代谢支持以及免疫细胞和血管生成的调节(图S5K)。因此,肠内营养供应对小肠生理学中各种细胞类型之间的协同作用产生了更为深远的影响。
通过分析转录因子(TF)结合基序,发现由脂肪酸激活并参与脂质代谢的关键TF,包括过氧化物酶体增殖物激活受体α(PPARα)及其伴侣维甲酸x受体(RXR),在BSF特异性OCR中富集(图6I)。研究人员对分选的小肠上皮细胞进行了染色质免疫沉淀(ChIP)测定,发现与其他位点相比,BSF诱导的PPARα结合在位点1(-2331至-2345 bp)显著增加(图6L)。相比之下,在LSF和DSF组中没有发现PPARα结合的这种诱导(图6M)。
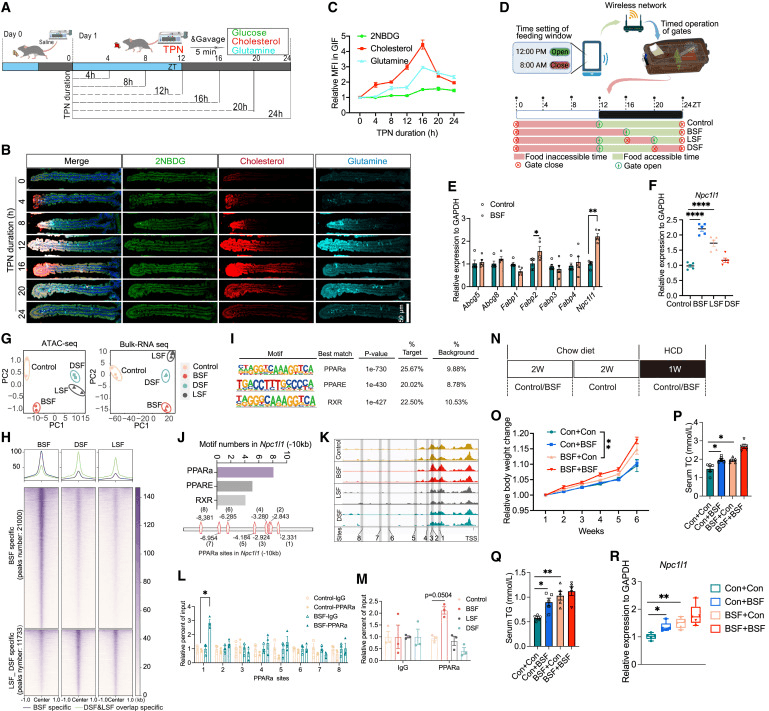
对GO项的进一步分析表明,与对照组相比,由BSF和BSF+对照组共同调节并位于这些共享OCR 50kb范围内的DEGs在与脂质吸收和代谢相关的方面显著富集(图S7L)。总之,在早餐的特定时间窗口内中断进食会通过重塑染色质可及性和招募相关的转录机制,引发小肠上皮细胞脂质吸收的持续适应性变化。
在美国和日本人群的队列研究中,不吃早餐与心血管疾病发病率增加有关,但其潜在机制尚不清楚。鉴于过量脂质摄取和积累在动脉粥样硬化等心血管疾病的病理中起着至关重要的作用,以BSF或对照喂养模式给易患动脉粥样硬化的Apo-E缺陷(Apoe-/-)小鼠喂食HCD 10周(图7A)引人注目的是,BSF导致Npc11l1的上皮表达及其从细胞表面向细胞质区域的内吞作用急剧增加(图7B),表明BSF条件下小肠对胆固醇的吸收增强。在全身水平上,尽管两组的食物摄入量相似(图7C),但BSF导致血清TG、TC和低密度脂蛋白胆固醇(LDL-C)水平升高,同时降低了排泄胆固醇的粪便水平(图7D和7E)。
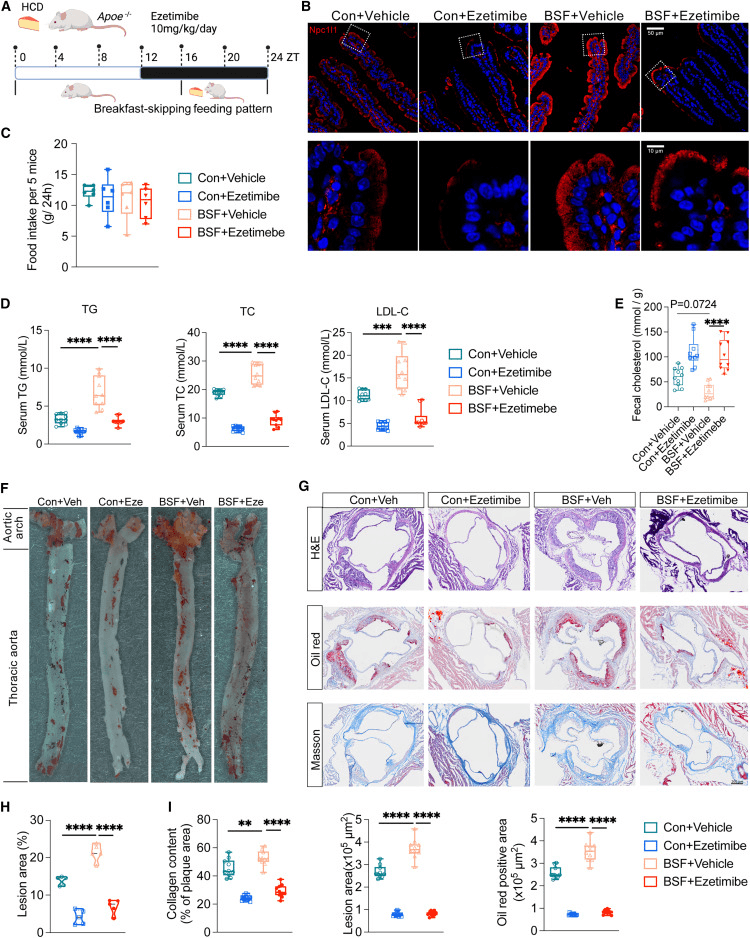
发现BSF诱导Npc1l1表达和内吞作用增加(图7B),全身胆固醇水平增加(图7D),排泄胆固醇减少(图7E)都得到了恢复。我们最终检查了动脉粥样硬化病变的形成,发现BSF导致动脉粥样硬化病变面积显著增加,这些病变中积累了更多的脂质和胶原蛋白,依折麦布仍然有能力预防这些病理变化(图7F-7I)。
数据表明,肠内营养供应总体上对肠上皮细胞的吸收(如刷状边缘组装和胆汁酸代谢)以及上皮屏障和周转有更大的影响,而浆膜供应似乎支持组织结构和细胞适应性。
这些发现为长期以来人们认为不吃早餐是一种不健康的生活方式提供了一种机械解释。有趣的是,间歇性禁食方案,包括限时进食(TRE),由于其代谢益处,在过去几年中越来越受欢迎。然而,研究强烈强调,虽然缩短白天的进食时间在一定程度上对代谢有益,但白天进食的具体时间窗口对TRE方案的净效果至关重要。
机制解读
不吃早餐导致小肠细胞脂质过度吸收,其核心机制:

01长时间空腹激活“营养危机”信号
当人体跳过早餐,经历约16小时的空腹(类似夜间禁食+早晨不进食),小肠长时间缺乏来自肠腔的食物营养。此时,身体误判为“食物短缺”,启动生存性适应机制。
02肠腔面营养缺失引发基因表达重编程
小肠上皮细胞对营养的吸收受“双向营养供给”调控:肠腔面(食物)和浆膜面(血液)。不吃早餐导致肠腔面营养长期缺失,而仅依赖血供营养维持。研究发现,这种不平衡会特异性上调脂质吸收相关基因,尤其是负责胆固醇吸收的NPC1L1基因,其表达水平显著升高。
03小肠进入“报复性吸脂”模式
一旦恢复进食,尤其是摄入含脂肪的食物,经过“重编程”的小肠细胞会过度吸收脂质和胆固醇,吸收效率远高于规律饮食者。这就像身体在“饥荒”后疯狂储存能量,优先将脂肪转化为体内储备。
04形成“代谢记忆”,影响持久
更令人担忧的是,这种脂质高吸收状态不会在恢复饮食后立即消失。实验显示,即使小鼠恢复正常进食两周,其小肠仍保持对脂质的“贪婪”吸收倾向,表明细胞层面形成了持久的“代谢记忆”。
长期后果:增加心血管疾病风险
过度吸收的脂质进入血液,导致血清中甘油三酯、总胆固醇和低密度脂蛋白(“坏”胆固醇)水平升高,同时粪便中排出的胆固醇减少,意味着更多胆固醇被身体吸收留存。长期积累会加剧动脉粥样硬化,增加心梗、中风等心血管疾病风险。
结束语
浙江大学的这项研究,让我们从分子层面认识到了不吃早餐对身体健康的潜在危害。它提醒我们,早餐不仅仅是一顿饭,更是维护肠道健康和代谢稳态的重要环节。在忙碌的生活中,我们应该重视早餐,养成规律进食的好习惯。毕竟,健康的身体是一切的基础,别让一时的疏忽,给未来的健康埋下隐患。从今天起,好好吃早餐,为自己的健康加分!
参考文献
1:A two-front nutrient supply environment fuels small intestinal physiology through differential regulation of nutrient absorption and host defense
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

