
2025年8月27日,法国图卢兹大学Nicolas Gaudenzio团队在Nature 在线发表题为“Maternal stress triggers early-life eczema through fetal mast cell programming”的研究论文,该研究表明,出生时的湿疹源自子宫内神经免疫回路的分子失调,这种失调是由母体下丘脑 - 垂体 - 肾上腺轴的波动所触发的。该研究发现,经历过压力的怀孕母鼠的后代存在失调的肥大细胞和皮肤伸展神经元,并且在面对无害的机械摩擦时会迅速出现湿疹。

01 研究过程
研究使用了PS7的非感染性小鼠模型,在该模型中,怀孕的母鼠被束缚并暴露在强光下30天 从胚胎第13天(E)到E18天,每天3次(图。 1a).PS方案对怀孕母鼠的体重、产仔数或出生后后代的体重没有影响(扩展数据图。 1a至c)。8周龄(W8)PS后代的皮肤在视觉和组织学上与对照(CT)后代相当,关键的宏观和微观特征没有可检测的变化,包括关键屏障蛋白的分布模式和丰度(图。 1b、 c和扩展数据图。 1d,e).W3和W8后代都表现出相对较高的经皮失水率(TEWL)(图。 1d和扩展数据图。 1f) 在稳态下,这是特应性皮炎,尤其是儿童,屏障松散的一个众所周知的功能指标8。在稳定状态下,W8后代的血清显示白细胞介素(IL)-7、CXCL9和2型细胞因子IL-5和IL-9的浓度增加(图。 1e).这些发现表明,尽管PS后代的皮肤看起来正常,但皮肤屏障发生了微妙的变化,这表明他们在稳定状态下容易产生2型免疫反应。
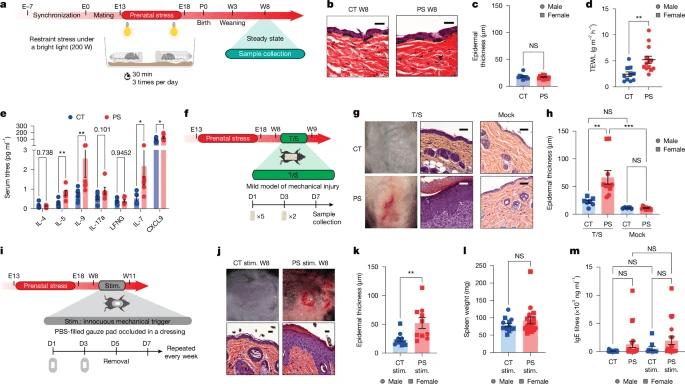
与W8相比,W24 PS后代仅表现出快速缓解的干燥,没有任何湿疹病变或表皮增厚的迹象(扩展数据图。 1s).总的来说,这些数据表明,这种PS模型与后代在无害的机械摩擦下发生湿疹样皮肤病变有关。病变表现出与成人特应性皮炎不同的病理特征,这种表型可以随着年龄的增长而自然消退
使用三种互补的行为检测方法评估了W8-PS后代的机械敏感性(图。 2a–c)与之前的研究结果一致,如图所示。 1f–k,发现在所有测试的行为实验中,PS后代的躯体机械敏感性明显高于CT后代(图。 2a–c和扩展数据图。 2a–c),表明暴露于PS后发生了机械超敏反应。接下来,我们分离了W8 CT和PS后代的DRG,并使用大量RNA测序(RNA-seq)进行了比较转录组分析(图。 2d).
为了研究不同人群中潜在的修饰功能反应,接下来在体外分离和培养DRG神经元(扩展数据图。 2d). 在PS后代的DRG中,对MRS2365有反应的神经元比例明显较高,而对β-丙氨酸和辣椒素的反应没有显著差异(扩展数据图。 2d).然而,两组反应神经元的反应幅度保持不变(扩展数据图。 2e–g)。
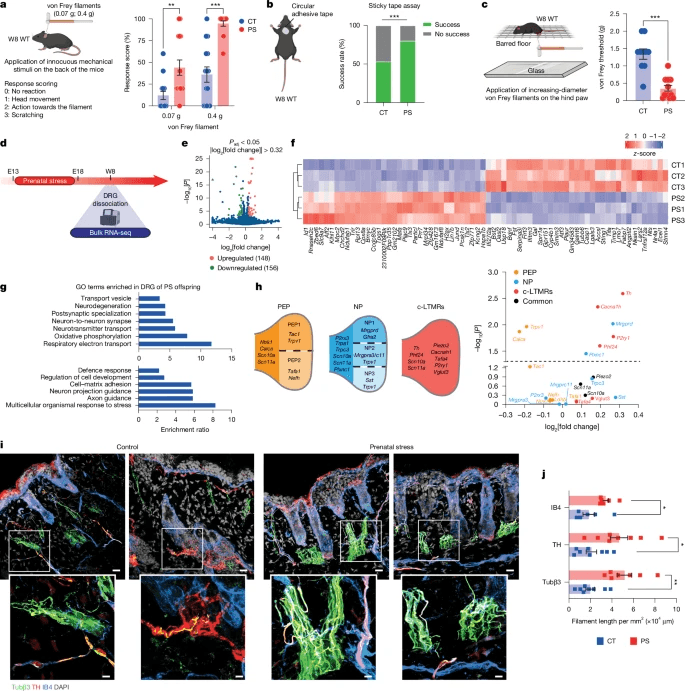
结果表明,PS与非肽能和c-LTMR神经元区室的转录组、功能和解剖结构改变以及对机械刺激的异常反应有关。
为了了解妊娠期间应激对皮肤驻留免疫细胞的潜在分子影响,使用荧光激活细胞分选(FACS)从W8和W24小鼠的皮肤中分离出CD45+免疫细胞(之前分别显示对轻度连续湿摩擦有反应和无反应;扩展数据图。 1r、 s)并进行单细胞RNA测序(scRNA-seq),以生成每个单个细胞的转录谱(图。 3a和扩展数据图。 4f). 在PS肥大细胞中丰富的其他基因本体术语中,我们发现了与应激相关的神经内分泌途径、氧化磷酸化和异常的免疫系统生理学(图。 3h).受压妊娠母鼠的皮肤驻留肥大细胞没有更多地脱颗粒(扩展数据图。 5a) ,表明观察到的表型仅限于胎儿组织。
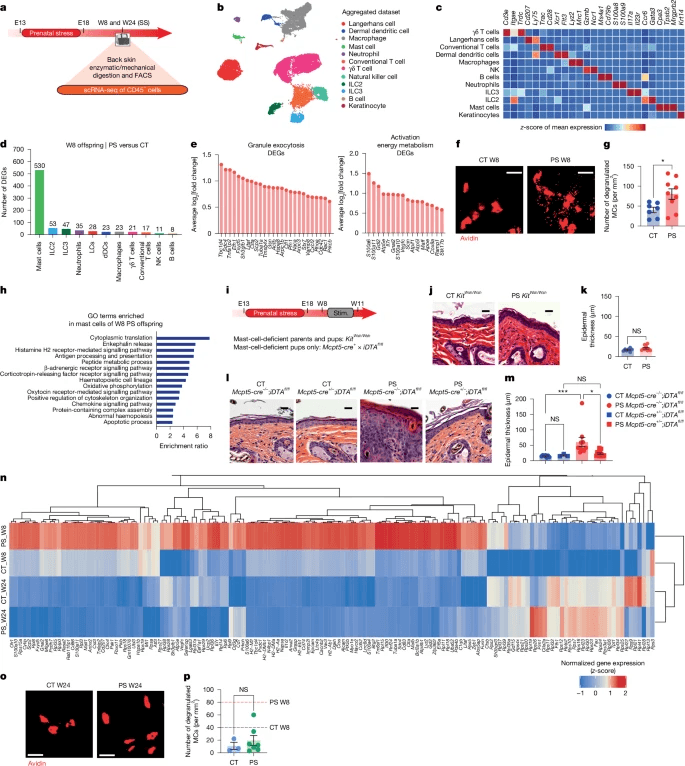
接下来给怀孕的Cdh5-creERT2+/−服用了单剂量的4-羟基他莫昔芬(4OHT);分别在E7.5或E10.5构建mTmG(细胞膜定位tdTomato(mT)和细胞膜定位EGFP(mG))母体,以定位卵黄囊衍生或造血干细胞(HSC)衍生的肥大细胞(扩展数据图。 5j).使用E18.5 PS胎儿厚胎儿皮肤切片的共聚焦成像,我们观察到大多数脱颗粒肥大细胞在E18.5时起源于卵黄囊,而只有少数来源于HSC(扩展数据图。 5k–m)。报告表明长寿命皮肤肥大细胞的自然周转率至少为24 第22、24、25周。总之,这些结果至少可以部分解释为什么PS过敏性皮肤表型在W24时自然逆转。
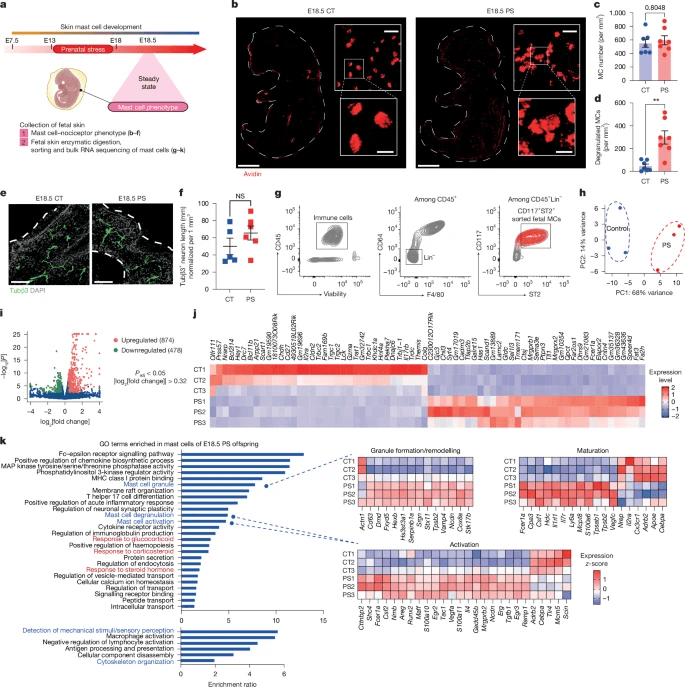
研究人员从四个E18.5 CT和PS胎儿的三个池中分选了胎儿皮肤肥大细胞(如CD45+CD64-F480-CD117+ST2+皮肤细胞)(图。 4g) 并进行了大量RNA-seq分析。PS胎儿的胎儿肥大细胞显示1284 DEGs(最小倍数变化大于1.25;Padj < 0.05),874个上调基因和478个下调基因(图。 4i,j).与W8的scRNA-seq数据集一致(图。 3e、 h),还观察到与糖皮质激素信号传导和神经元突触可塑性相关的基因强烈富集(图。 4k).总之,暴露于早期生活应激后,如此大的转录组修饰突显了子宫内胎儿肥大细胞发育/生物学的显著紊乱,包括颗粒形成、细胞活化/成熟和神经元调节所固有的基因。
为了研究皮质酮和/或富含皮质酮的羊水是否可以直接调节胎儿肥大细胞的活化。从E18.5胎儿皮肤中分选出CD117+肥大细胞,并在体外添加不同刺激物后监测肥大细胞脱颗粒动力学23(图。 5h).首先验证了实验框架,并观察到在添加P物质作为阳性CT后,胎儿肥大细胞的有效激活(图。 5i). 与载体CT相比,添加皮质酮导致平均荧光强度(MFI)显著增加,表明它可以直接作用于胎儿肥大细胞激活程序(图。 5j).与这一发现一致,来自PS卵黄囊而非CT的羊水也诱导了胎儿皮肤肥大细胞脱颗粒(图。 5j).
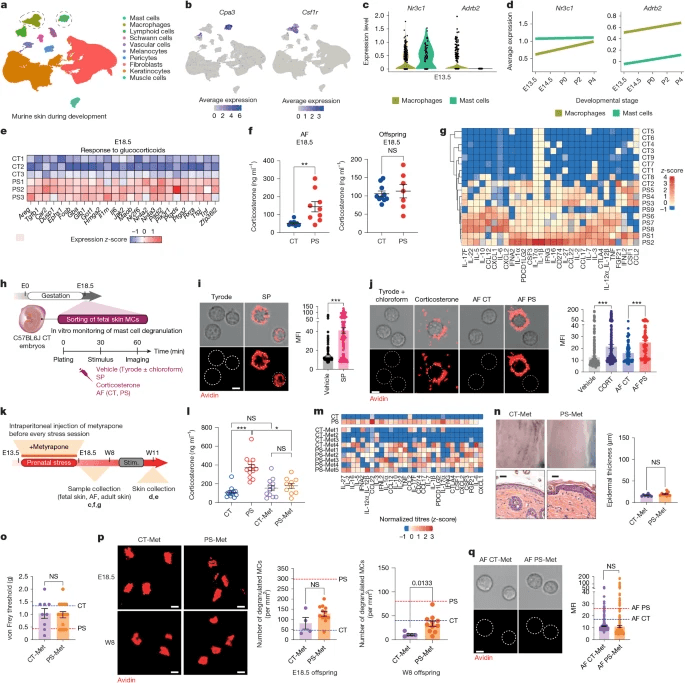
皮质酮浓度的短暂正常化防止了E18.5胎儿和W8成人皮肤肥大细胞的异常激活程序(图。 5p) ,这是PS相关表型所必需的现象(图。 3i–m)。经甲硫普酮处理的PS母鼠的羊水未能在体外激活胎儿肥大细胞,从而逆转了之前观察到的表型,并证实高浓度皮质酮的存在,而不是炎性细胞因子的存在,是导致胎儿肥大细胞激活的原因(图。 5q).
为了证实观察到的皮质酮对肥大细胞生物学的影响不仅是PS小鼠模型固有的,使用了转基因AdKOv2小鼠,其中Prkar1a(也称为Cnc1)的肾上腺特异性消融再现了促肾上腺皮质激素非依赖性库欣综合征的表型32(高皮质激素血症;扩展数据图。 6j).与同窝野生型CT相比,发现AdKOv2小鼠的皮肤表现出异常活化/脱颗粒的肥大细胞,这种表型与PS后代相似(扩展数据图。 6k).总之,在小鼠身上的发现表明,母体皮质酮分泌的增加会导致胎儿免疫程序的短暂改变,并在出生时产生湿疹病变的易感性。
总之,研究结果带来了一个新概念,即缓解的早发性湿疹可能起源于产前。有趣的是,推测出生时这种与PS相关的“脆弱”皮肤屏障可能有利于致病微生物的皮肤定植,国内过敏原的致敏,从而为所谓的特应性march铺平道路。更深入地了解母胎界面的微妙平衡可能会导致新的干预措施,以减轻怀孕期间环境因素的影响,最终降低儿童湿疹的极高发病率,并最终降低其他过敏性疾病的发病率。
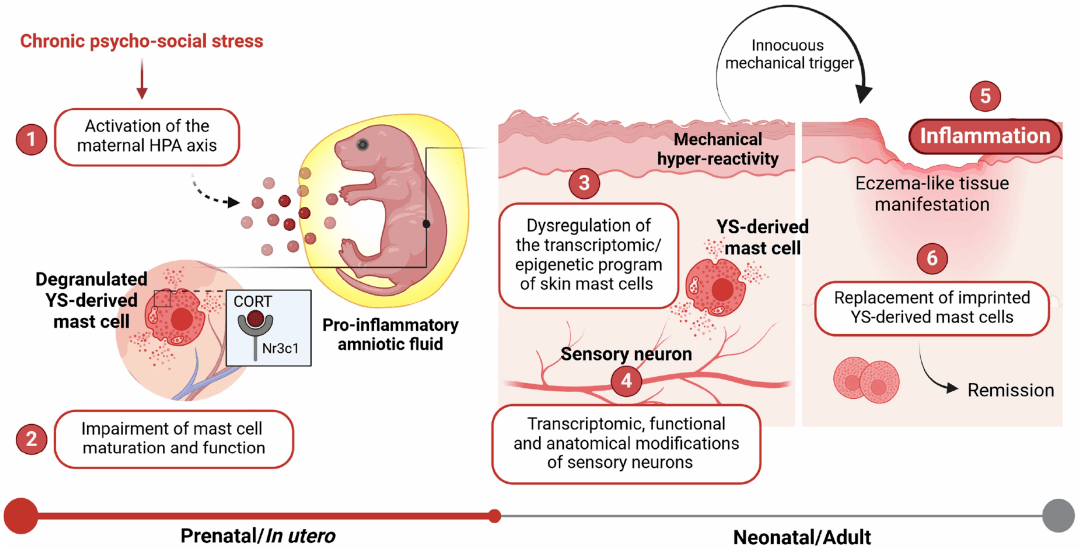
Nicolas Gaudenzio团队的研究不仅揭示了孕期压力诱发儿童湿疹的分子机制,还为临床干预提供了新的靶点。研究发现,在压力环境下妊娠期间,若能将母体皮质酮浓度恢复正常,或者通过基因手段减少Mcpt5 +肥大细胞的数量,就能防止胎儿免疫系统失调,并在出生后防止湿疹的发生。
02 孕期压力与儿童湿疹的隐秘关联
湿疹是一种以皮肤干燥、瘙痒和发炎为特征的皮肤病,在儿童时期较为常见,许多病例在出生后的第一年就开始出现。尽管湿疹与遗传、环境和免疫因素有关,但其在早期阶段的确切成因仍不清楚。

产前压力(PS)是指在怀孕期间反复接触令人厌恶的情况,包括高情绪压力,这被怀疑会影响婴儿的稳态系统。儿童湿疹在出生后受持续机械约束的弯曲部位迅速发展。流行病学研究就已反复暗示,母亲孕期的心理压力与孩子日后湿疹风险升高之间存在着某种神秘的联系。2003年,丹麦哥本哈根大学的研究团队对超过1.7万名母婴数据进行分析后发现,孕期经历重大生活事件(如亲人离世、婚姻破裂)的母亲,其子女在3岁前患湿疹的概率比普通儿童高出23%。后续的数十项跨国研究也不断重现类似结论,甚至有数据显示,孕期长期处于高压力状态的母亲,孩子青春期前发生特应性皮炎(湿疹的医学名称)的风险可增加近一倍。
03 对神经免疫系统的破坏机制
当肥大细胞发生异常编程,其释放的信号分子从“稳态调节剂”转变为“紊乱催化剂”,从多个层面破坏神经免疫网络的平衡:
1过度激活免疫炎症反应
异常编程的肥大细胞会持续大量释放组胺、白三烯等炎症介质,导致血管通透性异常增加,血浆外渗,引发皮肤红肿、风团等过敏症状。同时,它分泌的促炎细胞因子会招募更多免疫细胞浸润,放大局部炎症反应。在自身免疫性疾病中,这种过度活化还会导致免疫系统错误攻击自身组织,进一步加重组织损伤。
2扰乱神经-免疫双向对话
肥大细胞与神经末梢的双向调控是维持神经功能的关键,而异常编程会打破这种平衡。一方面,肥大细胞释放的组胺、类胰蛋白酶等介质会直接刺激感觉神经末梢,引发痛觉、痒觉异常,甚至导致神经源性炎症。
3损伤神经结构与功能
在代谢异常或慢性炎症状态下,异常编程的肥大细胞会释放大量炎症因子,直接损伤神经组织。在DPN小鼠模型中,高糖激活的肥大细胞会导致神经传导速度减慢、轴突密度降低、髓鞘大量脱落;而肥大细胞缺陷的小鼠,神经损伤程度则显著减轻。此外,肥大细胞释放的蛋白酶还会降解神经周围的基质成分,破坏神经的微环境支持,影响神经的修复与再生。
4影响中枢神经免疫稳态
近年来研究发现,肥大细胞还存在于脑膜、脉络丛等中枢神经系统区域,成为中枢神经免疫的“守门人”。当肥大细胞异常编程,其释放的组胺、5-HT等递质可透过血脑屏障,影响中枢神经元的功能,甚至参与情绪调节。例如,免疫细胞释放的细胞因子可作用于下丘脑,引发疲劳、抑郁等全身症状,而肥大细胞异常激活可能是这一过程的重要中间环节。
总 结
Nicolas Gaudenzio团队的这项研究,如同一把钥匙,打开了通往子宫内“压力密码”的大门,让我们首次清晰地看到了孕期压力如何通过分子机制影响胎儿的免疫系统发育,进而诱发儿童湿疹。这一发现不仅填补了产前应激与早发性湿疹之间生物学机制的空白,更为儿童湿疹的预防和治疗提供了新的思路和靶点。
参考文献
1:https://www.nature.com/articles/s41586-025-09419-8
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

