
2025年10月15日,纽约大学医学院Dan R. Littman团队在Nature 在线发表题为“Niche-specific dermal macrophage loss promotes skin capillary ageing”的研究论文,该研究表明,随着时间的推移,毛细血管相关巨噬细胞(CAMs)选择性丢失,导致老年小鼠血管修复受损和组织灌注减少。这项研究为理解皮肤老化的根本原因开辟了新视角,并为开发针对性的抗衰老策略提供了潜在的靶点。

01 皮肤衰老之谜
当我们谈论皮肤衰老时,常常想到的是皱纹、松弛和色斑。这些变化固然显著,但皮肤衰老是一个由内而外的复杂过程。皮肤的真皮层蕴藏着丰富的毛细血管网络,如同微小的生命线,负责向皮肤细胞输送氧气和营养,并运走代谢废物。维持这个微循环网络的健康和高效,对保持皮肤饱满、红润、富有弹性至关重要。然而,与外在的皱纹一样,皮肤内部的微血管网络也会随着时间流逝而退化、稀疏,功能下降,这种现象被称为“毛细血管衰老”。是什么驱动了这种微血管的老化?
02 研究过程
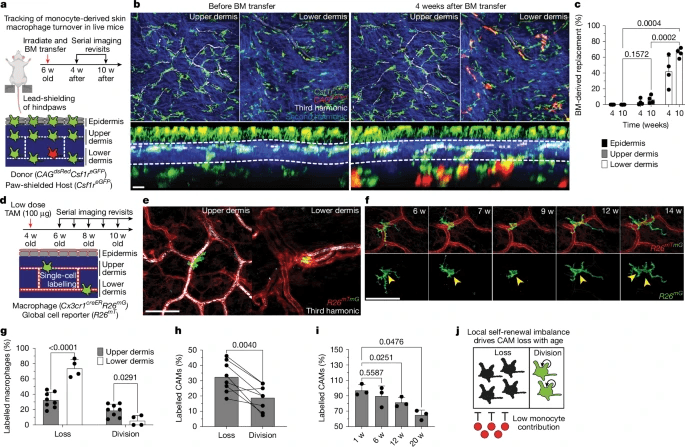
研究人员在活体小鼠中使用活体双光子显微镜对皮肤毛细血管丛进行无创成像,毛细血管丛是一个空间明确的血管生态位,随着年龄的增长而变得稀薄和功能下降。研究发现毛细血管与相关巨噬细胞的比例随着年龄的增长而显著降低(图1f)。CAM和覆盖率的下降速度超过了毛细血管的损失(扩展数据图3e,f),毛细血管先前被证明是小鼠和人类在多种组织中衰老的早期标志,包括中枢神经系统、肺、肾和皮肤。
观察结果表明,小鼠和人类的局部巨噬细胞损失可能导致毛细血管功能随着年龄的增长而受损。
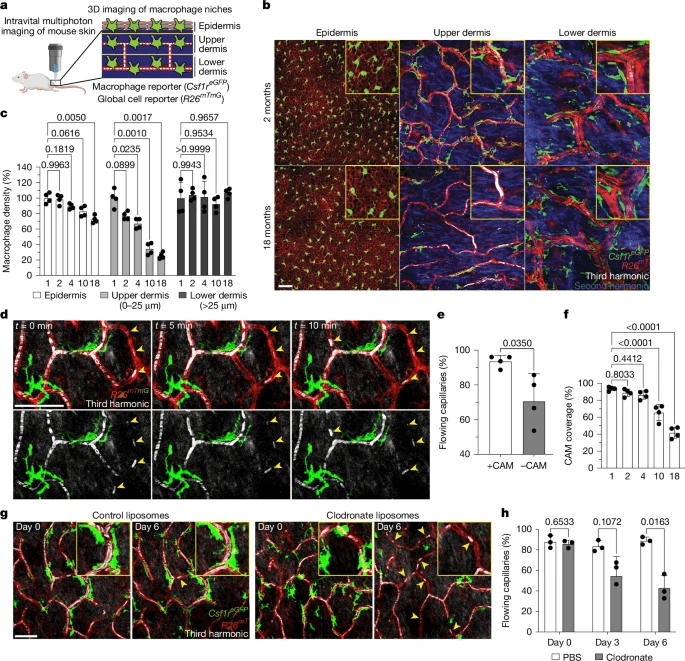
研究人员对1至7个月龄的Cx3cr1GFPR26mTmG小鼠进行了6个月的时间过程分析(扩展数据图5a),发现6个月龄小鼠的毛细血管注定要修剪 与维持的毛细血管相比,CAM覆盖率在一个月内有所下降(扩展数据图5b,c)。这一发现表明,随着年龄的增长,局部可能需要CAM来维持适当的毛细血管功能和保存。
研究人员进行了激光诱导凝血,发现与Cx3cr1GFP/+对照组小鼠相比,Cx3cr1GFP/GFP小鼠的CAM募集明显受损(扩展数据图5g,h)。我们还发现,CX3CR1缺乏导致血栓诱导后第7天毛细血管再灌注显著延迟和总体减少(扩展数据图5i)。接下来,我们评估了生理衰老过程中的毛细血管红细胞流量,发现6个月龄时,与Cx3cr1GFP/+对照组相比,Cx3cr1GFP/GFP小鼠的流动毛细血管明显减少(扩展数据图5j)。
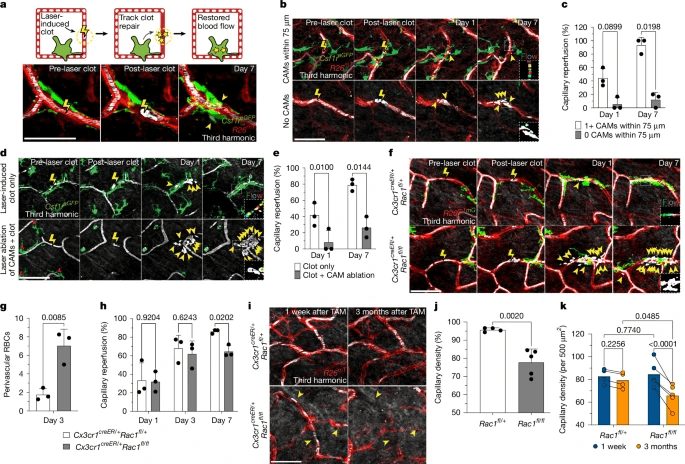
皮肤中组织驻留巨噬细胞群的维持被认为是通过局部增殖和骨髓(BM)来源的血液单核细胞的全身替代相结合来介导的13,41,42。为了了解CAMs在生理条件下是如何补充的,我们用Csf1reGFPCAGdsRed BM构建了BM嵌合体,并将其转移到致死性照射的Csf1reGFP小鼠体内。重要的是,这些小鼠的后爪被铅屏蔽,以防止我们的成像区域中的驻留巨噬细胞群丢失(图3a)。追踪10年内皮肤所有解剖层的巨噬细胞群 移植后几周,虽然大多数下层真皮巨噬细胞被单核细胞取代,但<5%的上层真皮巨噬细胞是BM衍生的(图3b,c)。
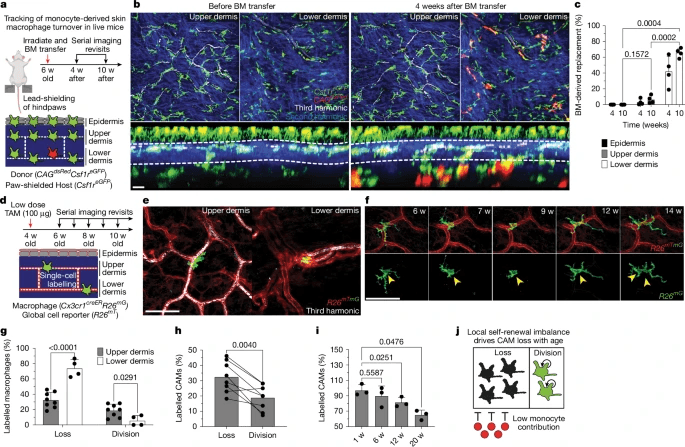
结果表明,CX3CR1+真皮巨噬细胞的自我更新策略具有生态位特异性,其中血液单核细胞募集用于真皮下部,局部细胞分裂用于真皮上部。重要的是,我们发现来自真皮上部的CAM没有得到局部增殖的充分补充,这导致了它们在这个组织生态位中的逐渐衰退(图3j)。
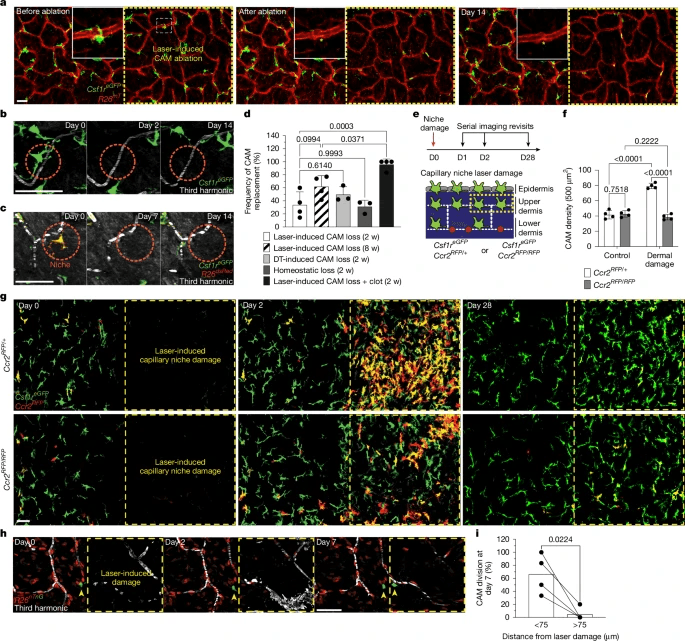
观察年轻(2个月大)和老年(10个月大的)小鼠中邻近CAM的分布来测试这一预测。在年轻小鼠中,大多数巨噬细胞在50 彼此相距µm。相比之下,老年小鼠的巨噬细胞模式呈双相分布,大多数CAM在25 µm或大于75 相距µm(扩展数据图9h)。这些结果突出了两个不同的细胞特征,这两个特征导致CAM覆盖率随着年龄的增长而降低:(1)CAM丧失后巨噬细胞再增殖不足;以及(2)这些细胞沿毛细血管生态位的再分配不足,这可能会促进血管网络的渐进性侵蚀(扩展数据图9i)。
研究发现激光诱导凝血后,这些相同区域的毛细血管修复明显改善(扩展数据图9m)。结果表明,老年小鼠的CAM在环境变化(如组织损伤)后可以稳定扩增。
研究人员在嵌合BM小鼠中进行了CSF1治疗,追踪局部和招募人群的相对扩张(扩展数据图10a,b)。与之前的实验一致,PBS注射的爪子成像区域没有显示出宿主或BM衍生巨噬细胞的显著增加(扩展数据图10c,d)。重要的是,发现CSF1诱导的CAM扩增并没有改变驻留(GFP+)和招募(GFP+dsRed+)CAM的比例(扩展数据图10e),因为GFP+dsRed+CAM相对于GFP+CAM的相对增加表明BM衍生的单核细胞招募。因此,这强烈表明CSF1推动了现有CAM种群的局部增殖。
值得注意的是,与PBS治疗的对照组小鼠相比,CSF1治疗足以改善老年小鼠的稳态毛细血管血流,后者的毛细血管段阻塞明显更多(图5d,e)。使用相同年龄的小鼠,接下来测试了CAM密度的增加是否足以提高毛细血管修复率。激光诱导凝血后,与PBS处理的对照组小鼠相比,CSF1处理的小鼠的毛细血管修复和再灌注有显著改善(图5f,g),表明恢复老年小鼠的皮肤巨噬细胞密度可以改善与年龄相关的血管功能障碍。
总的来说,研究揭示了一个衰老的连锁反应链:皮肤毛细血管旁的“守护者”巨噬细胞(CAMs)减少 → 毛细血管损伤修复不力 → 微血管网络退化、稀疏 → 皮肤组织供血供氧不足 → 促进皮肤结构破坏与功能衰老。
03 研究的发表具有里程碑式的意义
01 揭示皮肤衰老新机制
首次在活体动物中直接证明特定微环境下的巨噬细胞(CAMs)随年龄增长而流失,是驱动皮肤毛细血管衰老和组织功能退化(即皮肤整体衰老)的关键上游因素。
02 强调微环境重要性
凸显了组织微环境(血管生态位)在免疫细胞功能发挥中的决定性作用,以及特定位置免疫细胞亚群(如CAMs)在维持组织稳态中的不可替代性。
03 开创性研究方法
活体双光子显微镜的应用为研究复杂组织(如皮肤)中免疫细胞与血管、基质细胞的动态相互作用提供了强大工具,推动了衰老研究的深度。
04 潜在抗衰新策略
这项研究指出了一个潜在的全新抗衰老方向——针对毛细血管相关巨噬细胞(CAMs)。如果未来能开发出方法:
保护或延缓CAMs的流失(例如,理解其流失的分子信号并加以干预)。
增强或替代CAMs的功能(例如,通过特定药物或细胞疗法)。
就有可能维持或修复皮肤微血管网络,进而改善皮肤营养供给,延缓甚至逆转皮肤衰老的部分内在过程。
结 语
Dan R. Littman团队的这项研究,让我们对皮肤衰老的认识从表皮深入到了真皮微循环和免疫微环境的层面。它揭示了特定的免疫“守护者”——毛细血管旁巨噬细胞(CAMs)——的流失是皮肤衰老链条上的关键一环。这不仅深化了我们对衰老生物学的理解,更为未来开发**针对皮肤内在微循环衰老的新型干预措施**带来了希望。未来研究的重点将是深入探索CAMs流失的精确原因,寻找安全有效的干预手段来“守护这些守护者”,从而为对抗皮肤衰老、保持肌肤健康活力提供新的科学武器。
参考文献
1:Niche-specific dermal macrophage loss promotes skin capillary ageing
免责声明:本文旨在科普相关知识,不作为医疗指导意见
编辑|Zhang.ZG
审核|Geng.ZG

