
近日,一则令人痛心疾首的消息如巨石投湖,在社会中掀起轩然大波:一名年仅 20 岁的在读大学生,因长期饮食毫无规律,对煎炸炒烤食物情有独钟,且几乎与水果绝缘,竟被确诊为胃癌晚期。这一悲剧不仅让人为之惋惜,更如一声警钟,促使社会各界将目光聚焦于年轻人的健康状况。
在医疗领域,尽管当前胃癌(GC)的治疗手段日益多样化,但晚期胃癌患者的预后情况依旧不容乐观。因此,积极探寻具有高灵敏度与特异性的无创生物标志物、深度剖析胃癌发展的分子机制,并大胆探索创新疗法,对于提高胃癌诊断的精确度、增强治疗效果以及提升患者生存质量,有着至关重要的意义。
胃癌年轻化趋势严峻:数据背后的警示

国家癌症中心于 2024 年发布的全国癌症报告,为我们呈现了 2022 年中国新发癌症病例和死亡率的最新统计数据。其中,胃癌相关数据令人警醒:
胃癌发病与死亡数据:2022 年,中国胃癌新发病例约为 35.87 万,在所有癌症中位列第四,占新发癌症病例总数的 7.44%;死亡病例约为 26.04 万,在所有癌症中位居第三,占癌症死亡总数的 10.11%。
胃癌年龄分布:从年龄维度来看,胃癌在 0 - 34 岁年龄组的发病率和死亡率相对较低,然而,自 35 - 39 岁年龄组起便显著攀升,于 80 - 84 岁年龄组达到峰值。尤其值得注意的是,《2020 中国癌症患者生存质量白皮书》的数据表明,我国胃癌等多种癌症的年轻患者(15 - 39 岁)比例呈现出持续增加的趋势。
胃癌性别差异:在胃癌患者群体中,男性的发病率和死亡率均高于女性。
更令人担忧的是胃癌发病年龄的逐渐年轻化。据统计,19 - 35 岁青年人的胃癌发病率相较于 30 年前近乎翻了一番。这一趋势无疑向年轻人敲响了警钟:不良的生活习惯和饮食习惯,极有可能将他们推向严重疾病的深渊。
以这位 20 岁大学生为例,他长期熬夜、三餐不规律、饮食重油重盐且有吸烟喝酒等不良生活习惯,这些都是胃癌发生的高风险因素。更为关键的是,他长期对身体发出的早期预警信号,如胃部不适、食欲减退等置若罔闻,从而错失了最佳治疗时机。据统计,我国约 80% 的胃癌患者在确诊时已处于进展期或转移性胃癌阶段,早期治疗的黄金时期就这样被白白浪费。
外泌体在胃癌中的复杂角色:从机制到诊疗潜力
外泌体是一种由细胞内多囊泡体与细胞质膜融合后形成的特殊小囊泡,其呈杯状或盘状,直径介于 30 - 150nm 之间,能够主动分泌到细胞外。它们广泛分布于人体的各种体液之中,包括血液、唾液、尿液、脑脊液以及胸腹水等。外泌体最初被视作清除细胞内废物的 “垃圾袋”,但随着研究的深入,人们发现它在抗原提呈过程中有着重要作用,进而逐渐成为研究热点。
外泌体与胃癌的紧密关系:
肿瘤细胞相较于正常细胞,会分泌更多的外泌体。这些外泌体在细胞间穿梭往来,运输诸如蛋白质、核酸等各类生物学活性物质。当它们与靶细胞质膜融合后,便会释放内容物,从而改变靶细胞的表型。这种独特的机制实现了肿瘤与多种细胞间的信号和物质传递,在胃癌的发生、发展、转移、免疫逃避以及耐药性等一系列复杂过程中,都扮演着关键角色。
外泌体促进胃癌发展的多元机制:
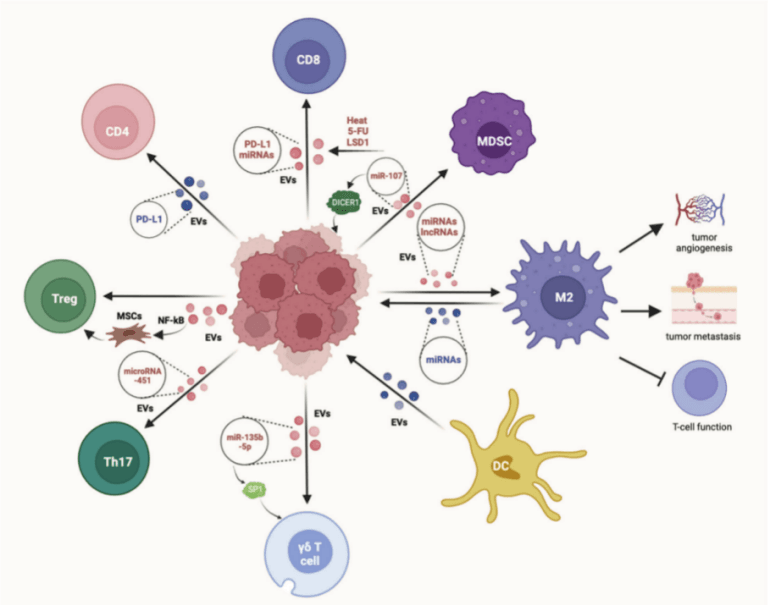
调控细胞信号分子:外泌体通过对细胞信号分子的精细调控,如 P53、PTEN、APC、TRIM3、miRNA 等,对胃癌细胞的生长和分裂产生影响。例如,P53 可通过提高 CAV1 和 CHMP4C 的表达来延缓肿瘤细胞生长和分裂;TRIM3 经外泌体介导转运至胃癌局部,发挥抑癌基因的作用,抑制胃癌细胞的增殖及迁移。然而,胃癌细胞来源的外泌体中某些 miRNA(如 miR - 423 - 5p)的过表达却会促进胃癌细胞的增殖。
促进肿瘤血管生成:肿瘤来源的外泌体富含血管相关生长因子,这些生长因子能够诱导血管生长相关因子基因的高表达,进而促进内皮细胞的增殖、迁移及出芽,为肿瘤的进展创造有利条件。例如,CD97 高表达的胃癌组织来源的外泌体具有促血管生成的作用,可提升胃癌细胞的增殖能力。
介导免疫逃避:外泌体在肿瘤细胞与免疫细胞之间的信息交流中发挥着关键作用,从而产生免疫抑制功能,助力肿瘤细胞实现免疫逃避。例如,巨噬细胞来源的外泌体中的 miR - 21 可直接转染至胃癌细胞,导致抑癌基因 PTEN 低表达,进而激活 PI3K/Akt 信号通路,抑制癌细胞凋亡。此外,肿瘤外泌体还可通过诱导髓系来源抑制细胞(MDSC)中 IL - 6 的自分泌,使 Stat3 磷酸化,最终激活 MDSCs 并触发其免疫抑制作用。
促进肿瘤转移:外泌体作为细胞间通讯的重要载体,是促进肿瘤转移癌基因和致癌因素传递的关键信使。它们能够将血管生成蛋白转运至内皮细胞,或者通过携带的 miRNA 调控内皮细胞的血管生成功能,从而促进肿瘤血管生长。此外,外泌体内容物(如促转移蛋白、miRNA 等)也能增强癌细胞的侵袭性。例如,外泌体内容物 Tetraspanin 8 与胃癌的侵袭及转移密切相关,并且成为胃癌预后评估的独立因子。
外泌体在胃癌诊断和治疗中的巨大潜力:
外泌体中蕴含着丰富的与癌症相关的蛋白、脂质、mRNA、非编码 RNA、DNA 等生物标志物,这些标志物为癌症检测提供了可能。由于外泌体体积微小,具备出色的穿越各种组织屏障(如血脑屏障)的能力,且广泛存在于各种体液中,易于获取和检测,因此在胃癌诊断方面有着巨大的潜力。在胃癌治疗领域,外泌体同样展现出了可观的潜力。例如,通过基因工程技术改造外泌体,使其表达特定的治疗分子或靶向蛋白,能够实现更为精准的治疗药物递送。此外,利用外泌体研发抗肿瘤疫苗也是当前研究领域的热点方向之一。
胃癌治疗的新曙光:新型手段与研究突破
面对庞大的胃癌患者群体,我们迫切需要更加高效、精准的诊疗手段来帮助他们战胜病魔。如今,除了传统的手术治疗、化疗和放疗手段外,越来越多的新型治疗方法如雨后春笋般涌现,免疫治疗、靶向治疗等逐渐崭露头角。这些新型治疗手段与外泌体等新型诊断方法相结合,有望为胃癌患者打造更加全面、个性化的治疗方案。
近年来,关于外泌体与胃癌的研究持续深入。例如,中山大学研究团队发现来自胃癌细胞的外泌体来源的 circATP8A1 通过 circATP8A1/miR - 1 - 3p/STAT6 轴诱导巨噬细胞 M2 极化和肿瘤进展。这一研究成果为胃癌的潜在预后生物标志物和治疗靶点开辟了新的思路。

中国医科大学第四附属医院魏房团队在《Cell Death and Disease》杂志上发表了题为 “Extracellular vesicles mediated gastric cancer immune response: tumor cell death or immune escape?” 的论著。该文章全面综述了胃癌细胞来源的 EVs 在免疫微环境重塑中的作用以及免疫细胞来源的 EVs 在胃癌发生发展中的作用,并对使用 EVs 的免疫治疗 GC 的潜在方法进行了概述。

呼吁与期待:守护健康,战胜胃癌
综上所述,外泌体在胃癌进程中扮演着多重复杂角色,包括促进胃癌细胞增殖与迁移、诱导胃癌血管生成、介导胃癌免疫逃避以及推动胃癌转移等。这些重要作用使得外泌体成为胃癌研究和治疗领域的关键靶点。展望未来,随着对外泌体研究的不断深入拓展,我们有理由相信,针对胃癌的新型诊断和治疗策略必将应运而生。
在此,我们向广大年轻人发出诚挚呼吁:务必时刻关注自身健康状况,坚决摒弃不良生活习惯,定期进行体检和肿瘤筛查。尤其是那些存在胃癌高危因素的人群,如曾感染幽门螺杆菌、有胃癌家族史、长期摄入高盐腌制食品等,更要尽早进行胃镜检查等相关检查,以便及时发现并治疗胃癌。
同时,我们也期待全社会能够齐心协力,高度关注胃癌等疾病的预防和治疗工作,为更多患者带来健康的希望之光。相信通过全社会的共同努力,我们一定能够战胜胃癌这一顽固病魔,让每一个年轻的生命都能在阳光下绽放出绚烂光彩!
参考文献
【1】Extracellular vesicles mediated gastric cancer immune response: tumor cell death or immune escape?Cell Death and Disease (2024) 15:377
【2】https://www.sciencedirect.com/science/article/pii/S2667005424000498
【3】Deng, C., Huo, M., Chu, H. et al. Exosome circATP8A1 induces macrophage M2 polarization by regulating the miR-1-3p/STAT6 axis to promote gastric cancer progression. Mol Cancer 23, 49 (2024).
编辑|Ning.ZG
审核|Geng.ZG

